下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
己知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O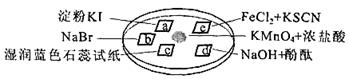
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+ > Cl- |
下列实验过程中,始终无明显现象的是 ( )
| A.Cl2通入AgNO3溶液中 |
| B.CO2通入CaCl2溶液中 |
| C.NH3通入AlCl3溶液中 |
| D.SO2通入Ba(NO3)2溶液中 |
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
| A.再通入少量氯气,c(H+)/c(ClO-)减小 |
| B.通入少量SO2,溶液漂白性增强 |
| C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) |
| D.加入少量固体NaOH,溶液的pH会略微增大 |
某同学用如图装置制备并检验Cl2的性质。下列说法正确的是( )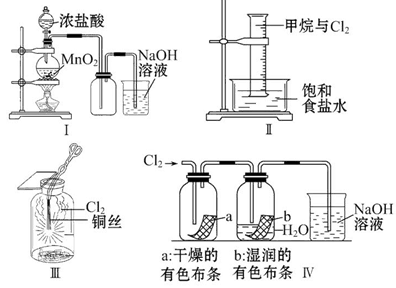
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗 |
| B.Ⅱ图中:量筒中发生了加成反应 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:湿润的有色布条能褪色 |
如图是一种检验某气体化学性质的实验装置,图中B为开关,如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
| A.浓硫酸 | B.饱和NaCl溶液 |
| C.浓NaOH溶液 | D.浓NaBr溶液 |
诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是( )
| A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸 |
| B.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅 |
| C.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆 |
| D.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应 |
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出)。
下列有关该方法的叙述中不正确的是( )
| A.能耗大是该方法的一大缺点 |
| B.整个过程中,可以循环利用的物质是CaO和NaOH |
| C.“反应、分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
| D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品 |
下列说法正确的是( )
| A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| B.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可 |
C.在粗硅的制取中,2C+SiO2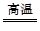 Si+2CO↑硅被还原,所以硅的非金属性比碳强 Si+2CO↑硅被还原,所以硅的非金属性比碳强 |
| D.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2 |
下列有关说法正确的是( )
| A.CO2、CH4、N2等均是造成温室效应的气体 |
| B. 14C可用于文物鉴定,14C与12C互为同素异形体 |
| C.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
D.精炼粗铝时要清除坩埚表面的石英砂,铝与石英砂反应的方程式为 |