如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O。对实验现象的“解释或结论”正确的是( )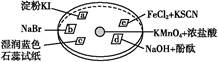
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
下列能够检验出KI中是否含有Br-的实验是( )
| A.加入足量的新制氯水,溶液颜色变深,则含有Br- |
| B.加入KMnO4酸性溶液,溶液颜色褪去,则含有Br- |
| C.加入少量的碘水,再加入CCl4振荡,CCl4层有色,则含有Br- |
| D.加入足量FeCl3溶液,用CCl4萃取后,在无色的水层中加入氯水,溶液呈橙黄色,则含有Br- |
二氧化硅(SiO2)又称硅石,是制备硅及其化合物的重要原料(见下图)。下列说法正确的是( )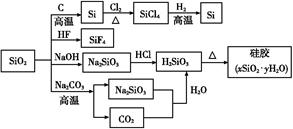
| A.SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 |
| B.SiO2和Si都是光导纤维材料 |
| C.在硅胶中加入CoCl2可显示硅胶吸水是否失效 |
| D.图中所示转化反应都是非氧化还原反应 |
取一定量的NaOH溶液通入CO2后,再继续向该溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,下列有关说法正确的是( )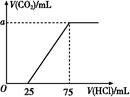
| A.原溶液中NaOH的物质的量为0.75 mol |
| B.通入CO2后所得的溶液溶质成分为NaOH和Na2CO3 |
| C.通入CO2后所得的溶液中含有2.5×10-3 mol NaHCO3 |
| D.纵坐标中a的数值为224 |
用4种溶液进行实验,下表中“溶液”与“操作及现象”对应关系正确的是( )
| 选项 | 溶液 | 操作及现象 |
| A | CaCl2溶液 | 通入CO2,溶液不变浑浊;再通入氨气,溶液变浑浊 |
| B | Na2SiO3溶液 | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊消失 |
| C | Ca(ClO)2溶液 | 通入CO2,溶液变浑浊;再加入品红溶液,红色不褪去 |
| D | BaCl2溶液 | 先通入NO2,再通入SO2至过量,先生成沉淀后沉淀消失 |
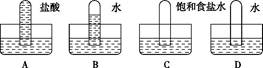
某同学为探究SO2与Ba2+只有在碱性条件下才能形成BaSO3沉淀,设计了如下方案,你认为可行的是( )
| A.将SO2通入Ba(OH)2溶液中观察有白色沉淀生成 |
| B.将SO2通入Ba(NO3)2溶液中观察有白色沉淀生成 |
| C.将SO2分别通入BaCl2溶液、BaCl2与HCl的混合溶液、Ba(OH)2溶液中,观察到只有Ba(OH)2中有白色沉淀生成 |
| D.将SO2通入BaCl2与NH3的混合溶液中有白色沉淀生成 |
由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
A.Mg Mg(NO3)2 Mg(NO3)2 |
B.Mg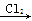 MgCl2 MgCl2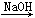 Mg(OH)2 Mg(OH)2 Mg(NO3)2 Mg(NO3)2 |
C.Mg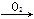 MgO MgO Mg(NO3)2 Mg(NO3)2 |
D.Mg MgSO4 MgSO4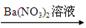 Mg(NO3)2 Mg(NO3)2 |
 低浓度 Br2
低浓度 Br2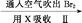 含Br-等的溶液
含Br-等的溶液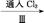 Br2的浓溶液
Br2的浓溶液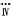 液溴
液溴 2Cl-+Br2
2Cl-+Br2