0 96731 96739 96745 96749 96755 96757 96761 96767 96769 96775 96781 96785 96787 96791 96797 96799 96805 96809 96811 96815 96817 96821 96823 96825 96826 96827 96829 96830 96831 96833 96835 96839 96841 96845 96847 96851 96857 96859 96865 96869 96871 96875 96881 96887 96889 96895 96899 96901 96907 96911 96917 96925 203614

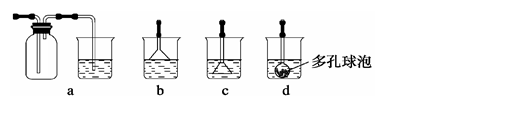
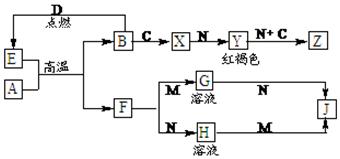
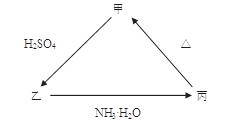
 丙的离子方程式______________________; 丙
丙的离子方程式______________________; 丙
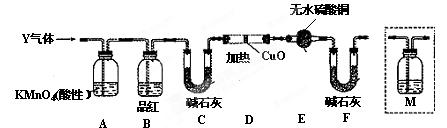
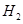 ,预计实验现象应是 。
,预计实验现象应是 。