钠与水反应的现象与钠的下列性质无关的是
| A.钠的熔点较低 | B.钠的密度小于水 |
| C.钠的硬度较小 | D.钠的还原性强 |
甲、乙两烧杯中分别盛有100mL 3.0mol·L—1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成气体体积比:甲∶乙=1∶2,则加入铝粉的质量为
| A.5.4g | B.3.6g | C.2.7g | D.1.8g |
将铜粉放入稀硫酸中,加热无明显变化,但加入某盐后发现铜粉质量明显减少,则该盐不可能是
| A.Fe2(SO4)3 | B.NaCl | C.KNO3 | D.Cu(NO3)2 |
下列物质中,既能跟盐酸反应又能跟氢氧化钠溶液反应的化合物是
| A.Al(OH)3 | B.NaAlO2 | C.AlCl3 | D.Al |
已知氧化性Fe3+>Cu2+。现将铜粉放入稀盐酸中,微热后无明显现象发生;当加入下列物质后,铜粉的质量减少。则加入的物质不可能是
| A.FeSO4 | B.Fe2(SO4)3 | C.KNO3 | D.HNO3 |
建筑用的钢材在出厂前都要经过烤蓝处理,使其表面生成一层四氧化三铁,其目的是
| A.增加钢材的硬度 | B.增强钢材的抗腐蚀能力 |
| C.使钢材美观 | D.增加钢材的韧性 |
15g铁粉和氧化铁的混合物,放入150mL稀H2SO4中,发现固体完全溶解,并放出1.68L H2(标准状况),加入KSCN溶液后,无颜色变化。为了使Fe2+完全转化为Fe(OH)2沉淀,共耗用200mL 3 mol/L NaOH溶液,则原硫酸溶液的物质的量浓度为
| A.4 mol·L—1 | B.3 mol·L—1 | C.2 mol·L—1 | D.1 mol·L—1 |
等体积、等物质的量浓度的稀硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为2:3,则甲、乙两烧杯中的反应情况可能分别是
| A.甲中酸过量,乙中碱过量 | B.甲中铝过量,乙中碱过量 |
| C.甲中酸过量,乙中铝过量 | D.甲、乙中都是铝过量 |
下列说法不正确的是
| A.用坩埚钳夹住一小块铝箔在酒精灯上加热到熔化,但熔化的铝并不滴落,是因为铝表面生成了熔点更高的氧化铝。 |
| B.铜属于重金属,它的化学性质不活泼,铜盐有毒,能使蛋白质失去活性,故误食铜盐后,应立即服用牛奶或蛋清急救再送医院治疗。 |
C.盐桥中通常装有琼脂的KCl溶液,形成如图所示原电池的闭合回路时,氯离子向正极移动,钾离子向负极移动。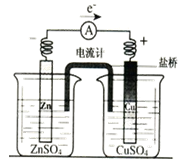 |
| D.水的电离是吸热反应,升高温度,促进水的电离,水的离子积常数Kw变大。 |
有 MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则原溶液中MgCl2、Al2(SO4)3的物质的量浓度之比为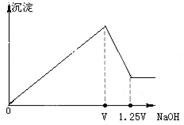
| A.1:1 | B.2:1 | C.3:2 | D.2:3 |