除去混在Na2CO3粉末中的少量NaHCO3,下列最合理的方法是
| A.加入适量NaOH溶液 | B.加热到固体质量不变 |
| C.加入适量HCl溶液 | D.加入适量CaCl2溶液 |
某课外活动小组做了一个有趣的实验:将2 g铝粉和3 g碘粉小心混合均匀,分为质量相等的3份,分别进行如下实验。现将实验记录列表如下,根据表中实验事实作出推断,其中正确的是(双选) ( )。
| 第一份 | 加入0.5 g水 | 很快产生火花 |
| 第二份 | 加入1 g胆矾 | 约需30 s产生火花 |
| 第三份 | 加入1 g无水硫酸铜 | 1 min时仍没有明显反应现象 |
A.水可能是起催化作用而增大铝与碘的化学反应速率
B.铝和碘不需任何条件即可发生化学反应生成AlI3
C.第一份和第二份实验中还可能观察到紫色的烟
D.第三份实验中是因为铝和硫酸铜发生了置换反应
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理: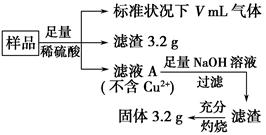
下列说法正确的是 ( )。
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B.样品中Fe元素的质量为2.24 g |
| C.样品中CuO的质量为4.0 g |
| D.V=896 mL |
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是 ( )。
| A.原子半径:Na>Al |
| B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na) |
| C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 |
| D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成 |
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1 HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法中不正确的是( )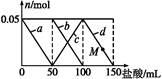
A.a曲线表示的离子方程式为:Al +H++H2O +H++H2O Al(OH)3↓ Al(OH)3↓ |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时,溶液中沉淀的质量为3.9 g |
D.原混合溶液中的C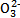 与Al 与Al 的物质的量之比为1∶2 的物质的量之比为1∶2 |
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是( )
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量CO2生成Al(OH)3沉淀 ⑤加入盐酸生成Al(OH)3沉淀 ⑥加入过量烧碱溶液
| A.①⑥⑤③ | B.②③④③ | C.②③⑤③ | D.①③⑤③ |
2013年2月15日早晨,一块陨石坠落在俄罗斯乌拉尔山脉地区,引发爆炸,造成1 000余人受伤,专家化验陨石碎片含铁10%。下列有关铁及其化合物的叙述中正确的是( )
| A.1 mol Fe分别与足量的盐酸或氯气反应电子转移数相等 |
| B.水蒸气与铁在常温下反应生成Fe3O4和H2 |
| C.Fe2O3和Al2O3都能溶解于NaOH溶液中 |
| D.生铁中的含碳量高于钢中的含碳量 |
常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,下列对所得溶液的描述不正确的是( )
| A.当1/2<a/b<1时,所得溶液中一定存在:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
| B.当a=b时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| C.当a/b=2/3时,所得溶液中存在:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| D.当2a=b时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
一定条件下,将Na与O2反应的生成物1.5g溶于水,所得溶液恰好能被80mL浓度为0.5 mol·L—1的HCl溶液中和,则该生成物的成分是
| A.Na2O | B.Na2O2 | C.Na2O和Na2O2 | D.Na2O2和NaO2 |