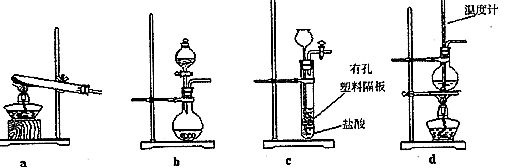
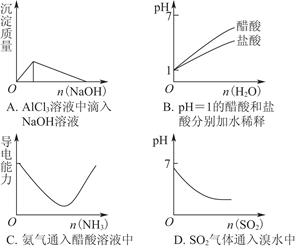
下列有关含铜化合物的说法错误的是(设NA为阿伏加德罗常数的值)
| A.用盐酸可以洗去铜表面的铜锈 |
| B.0.1mol/L的CuSO4溶液中,Cu2+的数目一定小于0.1NA |
| C.在CuCl2和FeCl3的混合溶液中加入铁粉,若有固体残留,则其中一定含有铜 |
| D.在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明Ksp(CuS)远小于Ksp(FeS) |
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是 ( )。
| A.原子半径:Na>Al |
| B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na) |
| C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 |
| D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成 |
向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,加水稀释,取少量所得溶液,加入少量二氧化锰,又有气体放出,待气体不再放出后,再滴加酚酞,溶液变红。下列猜测不合理的是
| A.过氧化钠和水反应生成氢氧化钠和氧气 |
| B.过氧化钠和水反应的产物是过氧化氢和氧气 |
| C.过氧化氢在二氧化锰催化作用下分解生成氧气和水 |
| D.过氧化钠跟水反应生成氢氧化钠和过氧化氢 |
可以用来检验碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )
| A.加热,看有无气体放出 |
| B.滴加盐酸,看有无气体放出 |
| C.溶于水后,滴加稀的氯化钡溶液看有无白色沉淀生成 |
| D.溶于水后,滴加澄清石灰水看有无白色沉淀生成 |
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是( )
| 选项 | 实验 | 现象 | 解释或结论 |
| A | 加入FeCl3固体 | 溶液变成红褐色 | FeCl3的水解程度变大 |
| B | 加入等体积水 | 溶液颜色变浅 | c(Fe3+)变小 |
| C | 加入足量Fe粉 | 溶液颜色变成浅绿色 | 2Fe3++Fe=3Fe2+ |
| D | 将FeCl3溶液微热 | 溶液变成红褐色 | 水解反应 ΔH>0 |
下列除杂所用的方法、试剂或发生的反应错误的是( )。
| A.除去FeCl2中的CuCl2:Fe+Cu2+=Fe2++Cu |
| B.除去Fe中的少量Al,可将固体加入到足量的NaOH溶液中,过滤 |
| C.除去FeCl2中的FeCl3:2Fe3++Fe=3Fe2+ |
| D.除去Fe2O3中的Fe(OH)3,可向混合物中加入足量的盐酸 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: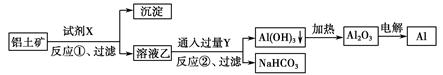
下列叙述正确的是( )。
| A.试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B.反应①、过滤后所得沉淀为氢氧化铁 |
| C.图中所示转化反应都不是氧化还原反应 |
| D.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 |
FeSO4可发生如图所示的一系列反应,下列说法错误的是( )。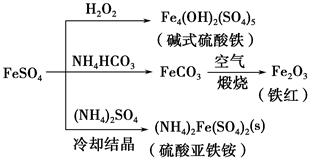
| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用做净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |