按图装置通入X气体,并在管P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是 ( )。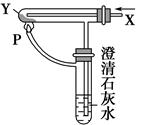
| A.H2和Fe2O3 |
| B.CO和CuO |
| C.H2和Na2CO3 |
| D.CO和Na2CO3 |
为了证明硫酸亚铁铵[(NH4)2Fe(SO4)26H2O]晶体的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
| A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH4+ |
| C.取适量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取适量硫酸亚铁铵晶体溶于水,得浅绿色溶液,滴入2滴KSCN溶液,溶液不显血红色,再滴入几滴新制氯水,溶液变为血红色,则可证明晶体的成分中含有Fe2+ |
如图是工业制纯碱的部分物质转化示意图,下列推测错误的是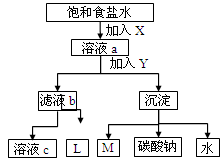
| A.若是联碱法,溶液c可在转化流程中循环利用 |
| B.若是氨碱法,则L的主要成分是NaCl |
| C.M可在转化流程中循环利用 |
| D.X是NH3,Y是CO2 |
1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
| A.Na2CO3 | B.Na2O2,Na2CO3 |
| C.NaOH,Na2CO3 | D.Na2O2,NaOH,Na2CO3 |
将5.4 g Al 投入到200mL 2.0 mol/L的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为
| A.HNO3溶液 | B.Ba(OH)2溶液 | C.H2SO4溶液 | D.HCl溶液 |
下列说法中,正确的是
| A.利用铁加入硫酸铜溶液中的反应可以比较Cu、Fe2+的还原性 |
| B.足量的铜跟一定量的浓硝酸反应只产生一种气体 |
| C.氮的固定只有在高温、高压、催化剂的条件下才能实现 |
| D.以铁为阴极、铜片为阳极、硫酸铜为电镀液可以实现铁制品镀铜 |
用铝热法还原下列氧化物制得金属各1 mol,消耗铝最少的是
| A.MnO2 | B.WO3 | C.Cr2O3 | D.Co3O4 |
下列关于100mL 0.1mol/L Na2CO3溶液叙述中不正确的是
| A.100mL 0.1mol/L Na2CO3溶液中含有CO32-的数目小于0.01NA |
| B.热的碳酸钠溶液比冷的碳酸钠溶液洗涤餐具效果好 |
| C.用碳酸钠除去锅炉中的水垢(主要成分是CaSO4),使之转化为疏松、易溶于酸的碳酸钙。 |
| D.100mL 0.1mol/L Na2CO3溶液中:n(CO32-)+n(HCO3-)+n(OH?)=0.01mol |
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6(相同状况),则甲、乙两烧杯中的反应情况可能分别是
| A.甲、乙中都是铝过量 | B.甲中铝过量,乙中碱过量 |
| C.甲中酸过量,乙中铝过量 | D.甲中酸过量,乙中碱过量 |
为了验证小苏打中是否含有纯碱,下列实验操作及方法正确的是
| A.观察加热时是否放出气体 |
| B.观察滴加盐酸时能否放出气体 |
| C.溶于水中,再滴加石灰水,观察有无沉淀产生 |
| D.溶于水中,滴加少量的氯化钡溶液,观察有无白色沉淀产生 |