下列离子方程式书写正确的是
| A.向氯化铵稀溶液中加入稀烧碱溶液 NH4+ + OH-=NH3↑+ H2O |
| B.氨水和硫酸反应 H+ + OH-=H2O |
| C.钠和水反应Na+ 2H2O= Na+ + 2OH-+ H2↑ |
| D.氯气与烧碱溶液反应Cl2+ 2OH-=Cl-+ ClO-+ H2O |
常温下,往NH4NO3溶液加人少量Na2O固体,溶液中微粒的数目不变的是
| A.NH4+ | B.H+ | C.NO3- | D.H2O |
下列离子在溶液中能大量共存,通入SO2气体后仍能大量共存的一组是
| A.NH4+、I-、Cl-、Ca2+ | B.K+、Na+、ClO-、SO42- |
| C.Fe3+、Na+、Cl-、SCN- | D.K+、Al3+、NO3-、AlO2- |
下表中有关离子方程式的评价合理的是 ( )
| 选项 | 化学反应及离子方程式 | 评价 |
| A | AlCl3溶液中加入过量氨水: Al3++3NH3·H2O=Al(OH)3¯+3NH4+ | 错误,铝元素的产物应该是AlO2﹣(或[Al(OH)4﹣]) |
| B | 过量氯气通入溴化亚铁溶液中: 3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2 | 正确 |
| C | 用氨水吸收过量二氧化硫: 2NH3·H2O+SO2=2NH4++SO32-十H2O | 正确 |
| D | 氯化铵溶于水: NH4+ + 2H2O = H3O+ + NH3·H2O | 错误,氯化铵溶解于水是物理变化,不能写离子方程式 |
下列离子方程式的书写正确的是
A.硫氢化钠溶液中滴人硫酸铜溶液: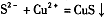 |
B.次氯酸钠溶液中加入双氧水有氧气产生: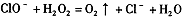 |
C.二氧化硫通入氯化铁溶液: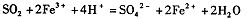 |
D.从酸化的海带灰浸出液中提取碘: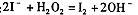 |
下列叙述或离子方程式书写正确的是 ( )
| A.将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+ClO-=SO42-+Cl-+2H+ |
| B.向含有Fe2O3悬浊液中通入HI气体: Fe2O3 + 6H+ = 2Fe3+ + 3H2O |
C.用惰性电极电解MgCl2溶液:2Cl- + 2H2O  Cl2↑+ H2↑+ 2OH- Cl2↑+ H2↑+ 2OH- |
| D.等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应: |
下列表示对应化学反应的离子方程式正确的是
| A.澄清石灰水中滴加少量的小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B.醋酸溶液和大理石中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C.NH4Al (SO4)2溶液中滴加少量的NaOH溶液:NH4++OH-=NH3·H2O |
| D.用氢氧化钠溶液除去铝表面的氧化膜:Al(OH)3+OH-=AlO2-+2H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使紫色石蕊试液变红的溶液:NH4+、Al3+、SO42-、Br- |
| B.明矾溶液:K+、C1-、S2-、OH- |
| C.pH=1的溶液:Ag(NH3)2+、Fe3+、ClO4-、NO3- |
| D.能溶解Al2O3的溶液:Na+、Mg2+、HCO3-、SO42- |
下列离子方程式中正确的是 ( )
A.用石墨作电极电解饱和NaCl溶液:2C1-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
B.向明矾溶液中逐滴加入Ba( OH)2溶液至Al3+刚好沉淀完全:Al3+ +SO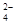 + Ba2+ +3OH- + Ba2+ +3OH- |
| C.过量氯气通人溴化亚铁溶液中2Cl2 +2Fe2+ +2Br- |
| D.向氯化铝溶液通入过量的氨气:Al3+ +4OH- |
常温下,下列各组离子在指定溶液中能大量共存的是 ( )
A.滴入酚酞显红色的溶液:Na+、Al3+、SO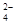 、Cl- 、Cl- |
B.滴入KSCN显红色的溶液:Na+、Cu2+、Br-、SO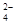 |
C.c( Fe2+)= 1mol·L-l的溶液:H+、Na+、Cl-、NO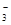 |
D.加入铝粉能产生大量H2的溶液:Na+、K+、Cl-、HCO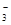 |