下列离子或分子在溶液中能大量共存,通NO2后仍能大量共存的一组是
| A.K+、Na+、Br-、SiO32- | B.H+、Fe2+、SO42-、Cl- |
| C.K+、Ca2+、Cl-、NO3- | D.K+、 Al3+、NH3·H2O、NO3- |
为确定某溶液的离子组成,进行如下实验:
①常温下,测定溶液的pH溶液呈强碱性;②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体;③在②反应后的溶液中再滴加Ba(NO3)2溶液,产生白色沉淀;④取上层清液继续滴加 Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。根据实验,以下对原溶液中大量存在的离子的推测正确的是
| A.一定含SO32- | B.一定含CO32- | C.C1-一定存在 | D.不能确定HCO3-是否存在 |
下列各组离子在溶液中能够大童共存,当溶液中的pH=1时,有气体产生;而当溶液中的pH=13时,又能生成沉淀。则该组离子可能是:
| A.Na+、K+、AlO2-、CO32- | B.Fe2+、Na+、SO42-、NO3- |
| C.Mg2+、NH4+、CO32-、Cl- | D.Ba2+、K+、Cl-、MnO4- |
下列离子方程式书写正确的是
| A.FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2=2Fe3+I2+4Cl- |
| B.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32- |
| C.向含有硫酸钙的水垢中加入碳酸钠溶液:CaSO4+CO32-=CaCO3+SO42- |
| D.等体积等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3↑+2H2O |
已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3·H2O。向含有等物质的量的NH4Cl、AlCl3和HCl混合溶液中慢慢滴加NaOH溶液至过量,并不断搅拌,可能发生以下离子反应:①H++OH-=H2O;②Al(OH)3+OH-=AlO2-+2H2O;③Al3++3OH-=Al(OH)3↓;④NH4++OH-=NH3·H2O;⑤NH4++AlO2-+2H2O=Al(OH)3↓+NH3·H2O。其正确的离子反应顺序是
| A.①③②④ | B.①③②⑤ | C.①③④② | D.①④③② |
下列有关离子方程式书写正确的
| A.向含1molFeI2溶液中通入标准状况下22.4LCl22Fe2+ + 2I- + 2Cl2 = 2Fe3+ + I2 + 2Cl- |
| B.向醋酸钠溶液中通入过量CO2 CH3COO- + CO2 + H2O →HCO3- +2 CH3COOH |
| C.向NaHSO4溶液中滴加Ba(OH)2溶液至中性2H++ SO42- + Ba2+ + 2OH- = BaSO4↓ + 2H2O |
| D.以金属银为阳极电解饱和硫酸铜溶液 Cu2+ + 2H2O=" 2Cu" + O2↑+ 4H+ |
下列方程式正确的是( )
A.用氯胺处理自来水:NH2Cl+H2O NH2OH+HCl NH2OH+HCl |
| B.在含有Mg2+、HCO3-的自来水中加入过量的澄清石灰水: Ca2+ +Mg2+ +2OH- +2HCO3-=CaCO3↓+MgCO3↓+2H2O |
C.长时间煮沸含Mg2+、HCO3-的自来水:Mg2+ +2HCO3-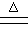 Mg(OH)2↓+2CO2↑ Mg(OH)2↓+2CO2↑ |
| D.Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为: |
下列状态的物质,既能导电又属于电解质的是
| A.MgCl2晶体 | B.NaCl溶液 | C.液态HCl | D.熔融的KOH |
BaSO4在熔融状态下能导电,其本质原因是
| A.是弱电解质 | B.存在离子 |
| C.存在电子 | D.存在自由移动的离子 |