室温下,强酸性和强碱性溶液中都不能共存的离子组是
| A.Ba2+、Fe2+、NO3-、I- | B.K+、Na+、SO32-、S2- |
| C.K+、Na+、AlO2-、SO42- | D.NH4+、Cu2+、Cl-、NO3- |
下列离子方程式书写正确的是
| A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 +3H+=Fe3+ +3H2O |
| B.在稀氨水中通入少量SO2:NH3?H2O+SO2=NH4++HSO3- |
| C.向澄清石灰水中加入足量NaHCO3溶液: Ca2+ +OH-+HCO3-=CaCO3↓+ H2O |
| D.在酸性KMnO4溶液中加入H2O2: 2MnO4-+5H2O2 +6H+=2Mn2++5O2↑+ 8H2O |
下列各组离子中可能大量共存的是
| A.在能使紫色石蕊试剂变红的溶液中:Na+、SO42-、Cl-、HCO3- |
| B.在强酸性溶液中:NH4+、Ba2+、Fe2+、Br-、NO3- |
| C.在含有大量AlO2-的溶液中:NH4+、Na+、Cl-、Al3+ |
| D.在水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、K+、CO32-、NO3- |
下列离子方程式书写正确的是
| A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+ H2O |
| B.标准状况下将112ml氯气通入6ml 1mol/L的碘化亚铁溶液中3Cl2+2Fe2++4I-=6Cl-+2Fe3++2I2 |
| C.漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+ 2HClO |
| D.向澄清石灰水中加入过量碳酸氢钠溶液Ca2++2OH-+2HCO3-=CaCO3↓+ 2H2O+CO32- |
下列表示对应化学反应的离子方程式正确的是
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
B.用铜为电极电解饱和食盐水:2Cl—+2H2O Cl2↑+H2↑+2OH— Cl2↑+H2↑+2OH— |
| C.硫酸亚铁溶液被空气中氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
| D.小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH—=BaCO3↓+2H2O+CO32— |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红色的溶液中:NO3-、SO42-、Fe2+、Na+ |
| B.强碱性溶液中:NH4+、NO3-、Ba2+、K+ |
| C.澄清透明的溶液中:MnO4-、Al3+、SO42-、K+ |
| D.含大量Fe3+的溶液中:Mg2+、Na+、Cl-、SCN- |
下列离子方程式中,正确的是
| A.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳: ClO-+CO2+H2O=HClO+HCO3- |
| B.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
| C.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+ |
下列热化学方程式或离子方程式中,正确的是:
| A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ·mol-1 |
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 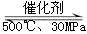 2NH3(g)△H=-38.6kJ·mol-1 2NH3(g)△H=-38.6kJ·mol-1 |
| C.氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH)2↓ |
| D.氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O=2Al(OH)4- |
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )。
| A.Fe3+、K+、Cl-、NO3- | B.Ag+、Na+、NO3-、Cl- |
| C.Zn2+、Al3+、SO42-、Cl- | D.Ba2+、NH4+、Cl-、HCO3- |
下列物质属于电解质的是( )
| A.干燥CuSO4 | B.CO2 | C.食盐水 | D.Fe |