下列表示对应化学反应的离子方程式正确的是:
| A.玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2O |
| B.硫酸亚铁溶液被空气中氧气氧化:4Fe2+ +O2+4H+=4Fe3+ +2H2O |
| C.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D.用食醋和淀粉-KI试纸检验碘盐中的KIO3IO3-+5I-+6H+=3I2+3H2O |
甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,下列说法正确的是
| A.甲为AlCl3,乙为NaHCO3 |
| B.溶液丙中还可以大量共存的离子有:Fe2+、NO3—、SO42— |
| C.在甲中滴加丁开始反应的离子方程式:HCO3—+ Ba2++OH—= BaCO3↓+ H2O。 |
| D.白色沉淀A可能溶解在溶液D中。 |
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )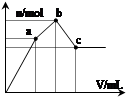
| A.a点的溶液呈中性 |
| B.b点到c点之间发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— =Al(OH)3↓+2BaSO4↓ |
| C.c点加入Ba(OH)2溶液的体积为200 mL |
| D.c点溶液呈碱性 |
下列设计与离子反应方程式书写均正确的是( )
A.磁性氧化铁溶于氢碘酸:Fe3O4+8H+ 2Fe3++Fe2++4H2O 2Fe3++Fe2++4H2O |
B.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2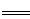 2NH4++SO32-+H2O 2NH4++SO32-+H2O |
C.用浓盐酸酸化的高锰酸钾溶液与过氧化氢反应:2MnO4- +5H2O2 + 6H+ 2Mn2+ +5O2↑ + 8H2O 2Mn2+ +5O2↑ + 8H2O |
D.用氨水洗涤试管内壁的银镜:Ag++2NH3·H2O [Ag(NH3)2]++2H2O [Ag(NH3)2]++2H2O |
向饱和石灰水中不断通入二氧化碳,其溶液导电性的变化是( )
| A.由弱变强 | B.由强变弱 |
| C.由强变弱,再变强 | D.由弱变强,再变弱 |
下列物质中含有自由移动的Cl―的是( )
| A.KClO3溶液 | B.液态HCl |
| C.KCl溶液 | D.NaCl晶体 |
下列说法中,正确的是
| A.溶于水的强电解质在水中完全电离 |
| B.强电解质在水中溶解度一定大于弱电解质 |
| C.强电解质一定是离子化合物 |
| D.强电解质溶液的导电性一定大于弱电解质 |
某物质的水溶液能导电,且该物质属于非电解质,溶于水时化学键被破坏的是
| A.液溴 | B.蔗糖 | C.干冰 | D.硫酸钡 |
下列物质能导电,且属于电解质的是
| A.二氧化硫的水溶液 | B.熔融态氯化钠 | C.铜 | D.冰醋酸 |
下列物质属于强电解质且能导电的是
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸
| A.⑤ | B.①②⑥ |
| C.②⑤⑥⑦ | D.①③④⑤⑥ |