下列示意图与对应的反应情况符合的是( )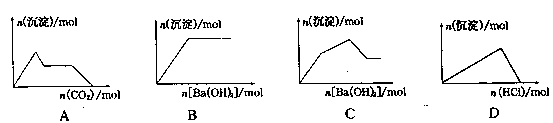
| A.向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 |
| B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 |
| C.向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 |
| D.向NaAlO2溶液中逐滴加入盐酸至过量 |
下列反应的离子方程式书写正确的是( )
| A.过量铁加入到稀硝酸中: 3Fe + 8H+ + 2NO3- = 3Fe2+ + 2NO↑ + 4H2O |
| B.向NaAlO2溶液中通入过量CO2: 2AlO2- + CO2+ H2O = 2Al(OH)3↓+ HCO3- |
| C.向AgC1悬浊液中滴加饱和NaI溶液: AgC1+I- ="AgI" + C1- |
| D.向KHCO3溶液中加入过量的澄清石灰水:2HCO3-+ Ca2++2OH-=CaCO3↓+CO32-+2H2O |
在水溶液中能大量共存的一组离子是( )
| A.Na+ Cl- NO3- H+ | B.Na+ Cu2+ Cl- S2- |
| C.K+ SO32- Fe3+ NO3- | D.K+ NH4+ SiO32- SO42- |
下列离子方程式的书写正确的是( )
| A.氢氧化钡溶液与等物质的量的稀硫酸混合:Ba2++2OH-+2H++SO42-==BaSO4↓+2H2O |
| B.向澄清石灰水中通入足量的CO2:CO2+Ca2++2OH-=CaCO3↓+H2O |
| C.高锰酸钾酸性溶液吸收二氧化硫:SO2+MnO4-+4H+=SO42-+Mn2++2H2O |
| D.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
常温下,下列各组离子在指定溶液中能大量共存的是 ( )
| A.由水电离的c(H+)=10-4mol/L的溶液中:Fe2+、SO42—、K+、NO3— |
| B.由水电离的c(H+)=10-14mol/L的溶液中:Ca2+、Na+、HCO3—、NO3— |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、SO42—、Cl— |
| D.c(Fe3+)=0.1mol/L的溶液中:Na+、K+、NO3—、SO32— |
下列实验设计及其对应的离子方程式均正确的是( )
| A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- |
| D.用稀硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
下列各组离子一定能大量共存的是( )
| A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.在强碱性溶液中:Na+、K+、AlO2-、CO32- |
| C.在c(H+)=10-13 mol/L的溶液中:NH4+、Al3+、SO42-、NO3- |
| D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
能正确表示下列反应的离子方程式为
| A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH–= CO32-+ H2O |
| B.二氧化硫通入次氯酸钠溶液:SO2 + ClO- + 2OH–= SO42-+Cl-+ H2O |
| C.硫化钡加入稀硫酸:BaS + 2H+ = H2S↑+ Ba2+ |
| D.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O="3I" 2+6OH- |
下列各组离子在指定条件下,一定能大量共存的是
| A.pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- |
| B.能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl- |
| C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- |
| D.能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、NO3- |
已知:(1)Al(OH)3的电离方程式为:AlO2-+H++H2O Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
(2)无水AlCl3晶体的沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:
PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
| A.均为强电解质 | B.均为弱电解质 |
| C.均为离子化合物 | D.均为共价化合物 |