下列有关铁及其化合物的离子方程式一定错误的是
A.氢氧化铁与氢碘酸反应:Fe(OH)3+3H+ Fe3++3H2O Fe3++3H2O |
B.铁与稀硝酸反应:Fe +4H+ + NO3- Fe3+ + NO↑+ 2H2O Fe3+ + NO↑+ 2H2O |
C.磁性氧化铁与浓盐酸反应:Fe3O4+8H+ 2Fe3++Fe2++4H2O 2Fe3++Fe2++4H2O |
D.溴化亚铁溶液与氯水反应:2Fe2++4Br-+3Cl2 2Fe3++2Br2+6Cl- 2Fe3++2Br2+6Cl- |
在水溶液中能大量共存的一组离子是
| A.H+、Na+、SO42-、SiO32- | B.Ba2+、Al3+、Cl-、SO42- |
| C.K+、Mg2+、SO42-、NO3- | D.H+、Fe2+、ClO-、NO3- |
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH—、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是
A.甲中一定含Na+ B.乙中一定含NH4+
C.丙中一定含Mg2+ D.丙中一定含SO42—
某溶液可能含有Na+、Ag+、Al3+、S2-、CO32-、SO32-、NO3-等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色。根据以上实验现象,下列关于原溶液中离子成分的推测正确的是
| A.一定有S2-、SO32-、Na+ | B.可能只有Na+、S2-、CO32- |
| C.一定没有Ag+、Al3+ | D.可能只有Na+、S2-、NO3- |
如图,将2 mL浓度为6 mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失。对该反应过程的推断不合理的是: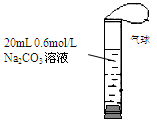
| A.有反应CO32- + 2H+ → CO2↑ + H2O发生 |
| B.有反应CO32- + H+ → HCO3-发生 |
| C.有反应CO32- + CO2 + H2O→ 2HCO3-发生 |
| D.加快盐酸注入速度不会改变反应现象 |
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、NH4+、Fe3+、 A13+、Cl―、OH―、NO3―、S2―、CO32―、SO42―。己知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是
| A.OH―、CO32―、SO42― | B.S2―、Cl―、SO42― |
| C.CO32―、NO3―、S2― | D.Cl―、SO42―、NO3― |
向明矾溶液中逐渐滴加Ba(OH)2溶液,可能发生反应的离子方程式为
| A.2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+ 3BaSO4↓ |
| B.Al3++SO42-+Ba2++3OH-→Al(OH)3↓+BaSO4↓ |
| C.2Al3++3SO42-+3Ba2++8OH-→2AlO2-+3BaSO4↓+4H2O |
| D.Al3++2SO42-+2Ba2++4OH-→AlO2-+2BaSO4↓+2H2O |
已知氧化性:Br2>Fe3+>I2,向含有a mol FeI2的溶液中加入含b mol Br2的溴水,下列判断或相应的离子方程式正确的是
| A.当a=2,b=1时,离子方程式为:2Fe2++Br2→2Fe3++2Br- |
| B.如果反应后的溶液中存在c(Fe2+)=c(Fe3+),则4/5<a/b<1 |
| C.当a=1,b=2时,离子方程式为:2Fe2++4I-+3Br2→2Fe3++2I2+6Br- |
| D.当a=2,2<b<3时,溶液中铁元素以两种离子形式存在,且一定是c(Fe3+)>c(Fe2+) |
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-(还原性SO32-大于I-),向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32-;④可能含有I-。
| A.①③ | B.①②③ | C.①② | D.②③④ |