常温下,在下列各组溶液中,加水稀释时c(H+)/c(OH-)明显增大,且能大量共存的离子组是( )
①K+、Cl-、NO3-、AlO2- ②K+、Fe2+、I-、SO42-
③Ba2+、OH-、NO3-、Na+ ④Na+、Ca2+、Al3+、Cl-
| A.①② | B.①③ | C.②④ | D.②③ |
下列离子方程式正确的是( )
A.碳酸氢钠水解:HCO3-+ H2O H3O+ + CO32- H3O+ + CO32- |
B.醋酸铵溶于水:CH3COONH4 + H2O CH3COOH + NH3·H2O CH3COOH + NH3·H2O |
C.硫酸钙悬浊液中加入碳酸钠:CaSO4(s) + CO32-(aq) CaCO3(s) + SO42-(aq) CaCO3(s) + SO42-(aq) |
| D.硫酸氢钠溶液中滴入氢氧化钡溶液呈中性:H++ SO42-+ Ba2++OH-====BaSO4↓+ H2O |
下列离子方程式正确的是(双选) ( )。
| A.氯化铁溶液中加入铜粉:2Fe3++Cu===2Fe2++Cu2+ |
| B.向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+===Fe2++2H2O |
| C.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42—===BaSO4↓ |
| D.向硫酸氢钠溶液中滴加Ba(OH)2溶液至中性:2H++SO42—+Ba2++2OH-===BaSO4↓+2H2O |
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO3—、⑥Cl-、⑦OH-。向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是 ( )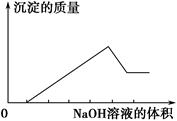
| A.①②⑤ | B.①③④ | C.②⑥⑦ | D.①②④⑥ |
下表所列各组第Ⅰ栏中的化学反应与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是 ( )。
| 选项 | 第Ⅰ栏 | 第Ⅱ栏 | 第Ⅲ栏 |
| A | 往少量NaOH溶液中投入铝片 | 往过量NaOH溶液中投入铝片 | 2Al+2OH-+ 2H2O===2AlO2— +3H2↑ |
| B | 往Fe2(SO4)3溶液中滴入NaOH溶液 | 往Fe2(SO4)3溶液中滴入Ba(OH)2溶液 | Fe3++3OH-===Fe(OH)3↓ |
| C | 往NaHCO3溶液中滴入Ca(OH)2溶液 | 往NaHCO3溶液中滴入NaOH溶液 | OH-+HCO3—====CO32—+H2O |
| D | 往NaOH溶液中通入过量CO2气体 | 往NaOH溶液中通入少量CO2气体 | CO2+OH-===HCO3— |
向含有下列各组离子的溶液中通入相应气体后,能大量共存的是( )。
| A.通入NO2:Na+、Fe2+、Cl-、SO42—42— |
| B.通入NH3:AlO2—=2—、NH4+、Na+、NO3—= |
| C.通入Cl2:K+、NH4+、I-、Cl- |
| D.通入CO2:Na+、K+、NO3—=、SiO3—= |
下列离子方程式正确的是 ( )。
| A.氢氧化镁与稀盐酸反应:H++OH-===H2O |
| B.AlCl3溶液中加入少量氨水:Al3++3OH-===Al(OH)3↓ |
| C.铜溶于稀硝酸:3Cu+8H++2NO3—===3Cu2++2NO↑+4H2O |
| D.次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO |
下面4组物质,能起反应,且既属于离子反应,又属于氧化还原反应的是( )
| A.Na2SO4溶液和BaCl2溶液 |
| B.铝片与Hg(NO3)2溶液 |
| C.稀硫酸与铜片 |
| D.NaNO3溶液与KCl溶液 |
下列分子或离子在指定的分散系中能大量共存的一组是( )
A.银氨溶液:Na+、K+、N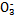 、NH3·H2O 、NH3·H2O |
| B.空气:C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体:H+、K+、S2-、Br- |
D.高锰酸钾溶液:H+、Na+、S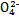 、葡萄糖分子 、葡萄糖分子 |
下列解释实验现象的反应方程式正确的是( )
| A.在CH3COONa溶液中,滴加酚酞溶液变红: CH3COO-+H2O  CH3COOH+OH- CH3COOH+OH- |
| B.在H2O2溶液中,滴加FeCl3溶液产生气泡: 2H2O2+2Cl-  2H2O+O2↑+Cl2↑ 2H2O+O2↑+Cl2↑ |
| C.将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生: Cu+2H+  Cu2++H2↑ Cu2++H2↑ |
| D.向Cu(OH)2悬浊液中滴加Na2S溶液,蓝色沉淀变黑色: |
 CuS(s)+2OH-
CuS(s)+2OH-