下列各组离子能大量共存的是( )
| A.pH<7的溶液中:Na+、S2-、K+、MnO4— |
| B.pH=7的溶液中:Al3+、Cl-、SO42—、AlO2— |
| C.pH>7的溶液中:Na+、CO32—、SO32—、K+ |
| D.pH=0的溶液中:Na+、Al3+、Fe2+、ClO- |
下列表示对应化学反应的离子方程式正确的是( )
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3—+3H2O=3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-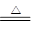 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3—+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3—=Ag++NO↑+H2O |
下列离子方程式正确的是( )
| A.利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
B.用铜为电极电解饱和食盐水:2Cl-+2H2O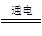 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.在明矾溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
| D.在小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH-=BaCO3↓+2H2O+CO32— |
已检测出pH=1的某未知溶液中含有Al3+和NO3—,若检验此溶液中是否大量存在以下6种离子:①ClO-②NH4+③Fe2+④K+⑤HCO3—⑥Cl-,其中不必检验就能加以否定的离子是( )
| A.①②⑥ | B.②③④ | C.①③⑤ | D.④⑤⑥ |
室温时,下列各组离子在指定溶液中可以大量共存的是( )
| A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、HCO3—、Cl- |
| B.无色透明溶液中:K+、Cu2+、SO42—、Na+ |
| C.含有大量AlO2—的溶液中:Na+、OH-、Cl-、CO32— |
| D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、SO42— |
能正确表示下列反应的离子方程式为( )
| A.碳酸氢钠溶液中滴入氢氧化钙溶液:2HCO3—+CO2++2OH-=CaCO3↓+CO32—+2H2O |
| B.二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42—+Cl-+H2O |
| C.硫化钡加入稀硫酸:BaS+2H+=H2S↑+Ba2+ |
| D.新制的氧化铝可溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2—+H2O |
下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl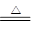 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
| C.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3—+Ca2++OH-=CaCO3↓+H2O |
下列说法正确的是( )
A.镁与极稀硝酸反应生成硝酸铵的离子方程式为:4Mg+6H++N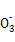 =4Mg2++N =4Mg2++N +3H2O +3H2O |
| B.常温下,0.1 mol/L一元酸HA溶液中c(OH-)/c(H+)=1×10-8,则此溶液的pH=3 |
| C.相同条件下,浓度均为0.01 mol/L的NH4Cl溶液和NaCl溶液中,前者的阳离子总浓度大于后者的阳离子总浓度 |
| D.物质的量浓度相等的醋酸和氢氧化钠溶液等体积混合后的溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(CH3COOH) |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是( )
A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、S |
B.b点对应的溶液中大量存在:N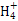 、Ba2+、OH-、I- 、Ba2+、OH-、I- |
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HC |
D.d点对应的溶液中大量存在:Na+、K+、S 、Cl- 、Cl- |