可溶性化合物A、B、C由下表中离子组合而成(每种离子只存在于一种化合物中)。
| 阳离子 | Mg2+、Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
现将等物质的量的A、B、C一起溶于水后,所得混合溶液中除H+、OH-外还含有五种离子。则A的化学式不可能是( )
A.AgNO3 B.Na2SO4 C.MgCl2 D.MgSO4
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
( )
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤、洗涤、灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中 ( )
| A.至少存在5种离子 |
| B.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1 |
| C.SO42-、NH4+一定存在,Cl-可能不存在 |
| D.CO32-、Al3+一定不存在,K+可能存在 |
下列叙述或表示方法正确的是( )
| A.Na2O2是离子化合物,其阴、阳离子个数比为1∶1 |
B.N(NO2)3(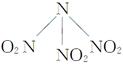 )既有氧化性又有还原性 )既有氧化性又有还原性 |
C.NH4HCO3溶液与过量的NaOH溶液微热反应:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.铜片溶于稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
下表中对离子方程式书写的评价错误的是( )
| 选项 | 化学反应与离子方程式 | 评价 |
| A | 将铜屑加入含Fe3+的溶液中:2Fe3+ +Cu=2Fe2++Cu2+ | 正确 |
| B | Na2O2与H2O反应:Na2O2+ H2O=2Na++2OH-+O2↑ | 错误,氧元素不守恒 |
| C | NaOH溶液与氧化铝反应:Al2O3+ 2OH-=2AlO2-+H2O | 错误,产物应该是Al(OH)3 |
| D | 向Fe(OH)2中加入足量稀硝酸: Fe(OH)2+2H+=Fe2++2H2O | 错误,HNO3能氧化Fe2+ |
下列离子方程式书写正确的是( )
| A.氢氧化镁与稀盐酸反应:H++OH-=H2O |
| B.向AlCl3溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ |
| C.铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D.向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
能正确表示下列反应的离子方程式是 ( )
| A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32-+H2O |
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O SO2↑+Cl2↑+H2O |
| C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
| D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓ |
下列离子方程式与所述事实相符且正确的是( )
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
下列离子方程式表达正确的是( )
| A.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| B.硫酸亚铁在空气中氧化:4Fe2++3O2+6H2O=4Fe(OH)3↓ |
| C.向氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O |
| D.碳酸氢镁溶液中加入足量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
下列化学反应的离子方程式正确的是( )
| A.在稀氨水中通入过量CO2:NH3·H2O+CO2=NH4++HCO3- |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C.用稀硝酸溶解FeS固体:FeS+2H+=Fe2++H2S↑ |
| D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-=CaSO4↓+H2O |