下列条件下,离子能大量共存或者离子方程式正确的是( )
| A.pH=1的溶液中:Fe2+、ClO-、Na+、SO42- |
| B.在含较多Al3+的溶液中:K+、Cl-、HCO3- |
| C.一小块钠投入到CuSO4溶液中:2Na+Cu2+= Cu+2Na+ |
| D.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2++ 2NO↑+ 4H2O |
常温下,下列各组离子能大量共存的是( )
| A.pH=12的溶液中:K+、Na+、Br-、AlO2- |
| B.无色溶液中:H+、K+、MnO4-、C2O42- |
| C.c(Fe3+) =" 0.1" mol·L-1的溶液中:K+、H+、SCN-、I- |
| D.由水电离出的c(OH-) =1.0×10-13 mol·L-1的溶液中:Na+、NH4+、SO42-、HCO3- |
下列离子方程式表达正确的是
| A.向氯化铁溶液中滴加HI溶液:2Fe3++2HI=2Fe2++2H++I2 |
| B.向NH4Al(SO4)2溶液中滴入Ba(0H)2恰好使反应完全:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O |
| C.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积均匀混合:2AlO2-+5H+=Al(OH)3↓+Al3++H2O |
| D.用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
根据表中信息,判断下列叙述中正确的是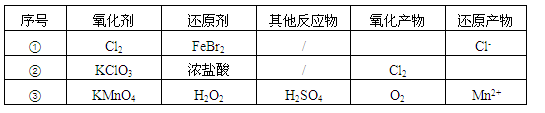
| A.表中①组的反应只可能有一种元素被氧化和一种元素被还原 |
| B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2 |
| C.由表中①②组反应推测:ClO3-、Br-、H+、Fe2+不能在浓溶液中大量共存 |
| D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 | B.Cl-一定存在,且c(Cl?)≥0.4 mol/L |
| C.SO42-、NH4+一定存在,Cl-可能不存在 | D.CO32-、Al3+一定不存在,K+可能存在 |
下列离子方程式正确的是
| A.氨气通入醋酸溶液:CH3COOH+NH3=CH3COONH4 |
B.亚硫酸氢钠溶液呈酸性:HSO +H2O +H2O H3O++SO H3O++SO |
| C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
D.稀硝酸洗涤试管内壁的银镜:Ag+2H++NO =Ag++NO↑+H2O =Ag++NO↑+H2O |
下列各组离子可能大量共存的是
| A.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH、S2-、Br- |
| B.遇pH试纸变红色的溶液:Fe2+、S2O、SO42-、Na+ |
| C.水电离出的c(H+) ?c(OH-) =10-28的溶液:Na+、S2-、NO3-、SO32- |
| D.能使KSCN显红色的溶液:Na+、NH4+、AlO、CO |
有一个未完成的离子方程式 +XO3-+6H+=3X2+3H2O。据此判断下列说法中正确的是
| A.X可能是周期表中第二周期元素 |
| B.X元素的原子最外层上有7个电子 |
| C.X2是还原产物,H2O是氧化产物 |
| D.若生成3 mol X2,转移6 mol电子 |
下列在指定溶液中的各组离子,能够大量共存的是
| A.使无色酚酞变红的溶液中:S2—、K+、CO32—、C1— |
| B.1mol·L—1的氯化铁溶液中:Na+、C1—、SCN—、Cu2+ |
| C.PH=0的溶液中:S2—、I—、Mg2+、Ba2+ |
| D.水电离的C(H+)=10—13mol·L—1的溶液中:Fe2+、SO42—、K+、NO3— |
下列各组离子在指定溶液中一定能大量共存的是
| A.含有Fe3+的溶液中:Na+、AlO2一、C6H5-、I- |
| B.含有大量NO3-的溶液中:H+、Na+、Fe3+、Cl- |
| C.加入Al能放出H2的溶液中:Cl-、NO3-、SO42-、K+ |
| D.由水电离出的c(OH—)=l×10—13mol?L—1的溶液中:Na+、Ba2+、Cl-、NH4+ |