下列说法正确的是:
①Cl-的结构示意图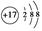 ;
;
②羟基的电子式: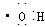 ;
;
③HClO的结构式:H—Cl—O;
④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化( )
| A.①②⑤ | B.①④⑥⑦ | C.②③④⑥ | D.②③⑤⑥⑦ |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| B.78 g 苯含有C="C" 双键的数目为3NA |
| C.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |
下列有关化学用语表示和概念判断叙述正确的是
| A.1molH2燃烧放出的热量为H2的燃烧热 |
B.氢氧根离子的电子式: |
C.氯原子的结构示意图: |
D. 和 和 互为同系物 互为同系物 |
设阿伏加德罗常数为NA,下列说法正确的是( )
| A.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA |
| B.1 mol NH3含有的电子数10NA |
| C.常温常压下,22.4L的氧气含氧原子数为2NA |
| D.常温下,1L0.1mol/L AlCl3溶液中含Al3+数为0.1NA |
下列化学(或离子)方程式正确的是
A.乙酸与碳酸钠溶液反应:2H++CO =CO2↑+H2O =CO2↑+H2O |
B.C6H6+HNO3 C6H5NO2+H2O C6H5NO2+H2O |
C.亚硫酸的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
| D.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→ CH3COO-+H2O |
下列化学用语正确的是
A.聚丙烯的结构简式: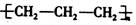 |
B.丙烷分子的比例模型: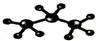 |
C.四氯化碳分子的电子式: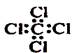 |
| D.甲烷结构简式为CH4 |
向18.4 g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成NO2、NO混合气体,再向所得溶液中加入足量的NaOH溶液,生成30.3 g沉淀。另取等质量的合金,使其与一定量的氯气恰好完全反应,则氯气的体积在标准状况下为
| A.7.84L | B.6.72L | C.4.48L | D.无法计算 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol Na2O2固体中含离子总数为4NA |
| B.标准状况下,22.4 L己烷中共价键数目为19NA |
| C.由乙烯和环己烷组成的混合物28g,含电子数为16NA |
| D.1 L浓度为1 mol·L-1的Na2CO3溶液中含有的CO32-数为NA |
向三份同浓度的25mL盐酸中分别加入质量不等的NaHCO3、KHCO3的混合物,测得产生
气体的体积如下表所示(不考虑气体溶解)
| 编号 | 1 | 2 | 3 |
| m(混合物)/g | 4.6 | 7.2 | 7.9 |
| V(CO2)(标准状况)/L | 1.12 | 1.68 | 1.68 |
下列分析推理正确的是
A.根据实验1中的数据可以计算出盐酸的浓度
B.混合物中NaHCO3的质量分数约为45.7%
C.根据第2、3组数据可以分析出第2组中的混合物完全反应
D.盐酸的物质的量浓度为1.5mol.L-1
今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4 mol·L-1的FeCl3溶液(其它用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变):
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
下列结论正确的是( )
A.第①组反应后溶液中c(Fe3+) =" 3.0" mol·L-1
B.第②组剩余固体是铜铁混合物
C.第④组反应后的滤液中c(Fe2+) =" 6" mol·L-1
D.原混合粉末中n(Fe)∶n(Cu) = 3∶2