0.8g某物质含有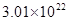 个分子,该物质的相对分子质量约为
个分子,该物质的相对分子质量约为
| A.8 | B.16 | C.64 | D.160 |
设NA代表阿伏加德罗常数,下列叙述正确的是 ( )
| A.标准状况下2.24 L H2O中,分子数为0.1NA |
| B.将1mol Cl2通入到水中,则N(HClO)+ N(Cl?)+ N(ClO-)= 2NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B.标准状况下,22.4L水的分子数为NA |
| C.将标准状况下11.2L的Cl2通入足量水中发生反应,转移的电子总数为NA |
| D.1mol/LK2SO4溶液所含K+数目为2NA |
用1L1mol·L-1NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为( )
| A.1︰3 | B.1︰2 | C.2︰3 | D.3︰2 |
现有CuO、FeO、Fe2O3组成的混合物m g,向其中加入100mL 3mol·L-1硫酸,恰好完全溶解,若mg该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为
| A.(m-1.6)g | B.(m-2.4)g | C.(m-4.8)g | D.无法计算 |
在标况下,下列气体含有的分子数最多的是
| A.36.5g HCl | B.4 mol H2O | C.4g H2 | D.0.5mol SO2 |
150℃时, NH4HCO3分解为NH3、H2O、CO2三种物质,此时混合气的密度是相同条件下的氢气密度的大约
| A.26.3倍 | B.15.25倍 | C.13.2倍 | D.12倍 |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A.现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3∶2∶1 |
| B.5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
同温同压下,等质量的SO2气体和SO3气体相比较,下列叙述中正确的是( )
| A.密度比为4:5 | B.物质的量之比为4:5 |
| C.体积比为1:1 | D.原子数之比为3:4 |
