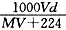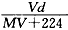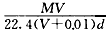下列所得溶液的物质的量浓度等于0.1 mol·L-1的是
| A.将0.1 mol氨气充分溶解在1 L水中 |
| B.将10g 1 mol·L-1的硫酸与90 g水混合 |
| C.将8g三氧化硫溶于水并配成1 L溶液 |
| D.将16g CuSO4·5H2O溶于水并配成1 L溶液 |
下列溶液中的氯离子数目与50 mL 1 mol·L-1的AlCl3溶液中氯离子数目相等的是
| A.150 mL 1 mol·L-1的KClO3 | B.150 mL 3 mol·L-1的KCl |
| C.75 mL 2 mol·L-1的CaCl2 | D.75 mL 2 mol·L-1的NH4Cl |
NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,NA个分子所占的体积约为22.4 L |
| B.标准状况下,2.24L CH4和NH3混合气体中含有的电子数目为NA |
| C.0.1 mol·L-1的K2SO4溶液中阴、阳离子总数为0.3NA |
| D.标准状况下,22.4L氢气和氦气混合气体中含有的原子总数为2NA |
由以下两种途径制铜:(1)CuO CuSO4
CuSO4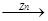 Cu (2)Zn
Cu (2)Zn H2
H2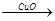 Cu 假设每一步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法正确的是
Cu 假设每一步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法正确的是
| A.消耗等物质的量的Zn、H2SO4、CuO |
| B.所有反应类型都相同 |
| C.过程中产生的ZnSO4质量相同 |
| D.只有CuO消耗的质量相同 |
如图所示装置,室温下密闭容器内分别充入空气和H2.O2的混合气体在可移动的活塞两边,在标准状况下若将H2.O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2.O2的体积比最接近于 ( )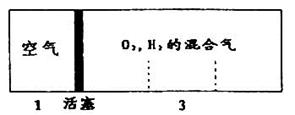
①2:7 ②5:4 ③4:5 ④7:2
| A.①② | B.②④ | C.③④ | D.①③ |
现有装有物质的量浓度为1.2 mol/L的盐酸100ml的容器甲和装有物质的量浓度为1mol/L的硫酸100ml的容器乙,向甲.乙容器内加入相同质量的铝,充分反应后生成氢气的体积比为3:4(标准状况下),问所加入的铝的质量是( )
| A.1.08克 | B.1.44克 | C.1.8 克 | D.无法计算 |
乙醇(C2H6O)水溶液中,当乙醇分子和水分子中氢原子个数相等时,溶液中乙醇的质量分数为( )
| A.20% | B.50% | C.46% | D.32% |
现有CO.CO2.O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的物质的量之比为( )
| A.1∶1∶1 | B.1∶2∶3 | C.3∶2∶1 | D.6∶3∶2 |
某氯原子的质量为a g,12C原子的质量为b g。用NA表示阿伏加德罗常数,下列说法中不正确的是
A.ng该氯原子所含的电子数为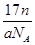 |
B.mg该氯原子的物质的量为 mol mol |
C.该氯原子的相对原子质量为 |
| D.0.5 mol该氯分子的质量为aNAg |