下列化学用语使用正确的是
A.Mg2+结构示意图: |
B.质子数为92,中子数为146的U原子: |
C.NH4Cl的电子式: |
D.四氯化碳分子球棍模型:  |
Cu、Cu2O和CuO组成的混合物,加入100 mL 0.6mol/LHNO3溶液恰好使混合物溶解,同时收集到224 mLNO气体(标准状况)。下列说法不正确的是
| A.产物中硝酸铜的物质的量为0.025 mol |
| B.若混合物中Cu的物质的量为0.005 mol,则其中Cu2O、CuO的物质的量共0.020 mol |
| C.若混合物中含0.01moLCu,则其中Cu2O、CuO的物质的量均为0.005 mol |
| D.混合物中Cu的物质的量的取值范围为0.005mol<n(Cu)<0.015mol |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.25°C时,1L pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA |
| B.室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2.0NA |
| C.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| D.标准状况下,22.4LCCl4中含有的分子数目为NA |
设NA为阿伏加德罗常数。下列叙述不正确的是
| A.标准状况下,22.4 L O3含有分子的数目为NA |
| B.常温常压下,4.0 g CH4中含有共价键的数目为NA |
| C.常温常压下,1 L 0.1 mol·L-1 NH4NO3溶液中NH4+、NO3-的数目均为0.1NA |
| D.标准状况下,2.24 L Cl2与足量NaOH溶液反应,转移电子的数目为0.1NA |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A.1 mol NH3中含有中子数为7NA个 |
| B.标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C.2 g氢气所含质子数是NA |
| D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
化学用语是学习化学的重要工具。下列化学用语错误的是 ( )
A.碳酸钠的水解反应:CO32-+H2O 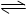 HCO3-+OH- HCO3-+OH- |
B.FeCl3水解的离子方程式:Fe3++3H2O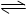 Fe (OH)3+3H+ Fe (OH)3+3H+ |
| C.稀溶液中强酸与强碱的中和热:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ· mol-1 |
| D.C燃烧的热化学方程式为:C(s)+1/2O2(g)=CO(g)△H = 110.5kJ·mol-1 |
下列说法正确的是( )
| A.0.5mol SO2和11.2LCO2所含的分子数目一定相等 |
| B.25℃和100℃时,水的pH相等 |
| C.中和等体积、等物质的量浓度的NaOH和氨水所消耗的n(H2SO4)相等 |
D.2SO2(g)+O2(g) 2SO3(g) 和4SO2(g)+2O2(g) 2SO3(g) 和4SO2(g)+2O2(g) 4SO3(g)的△H相等 4SO3(g)的△H相等 |
已知等体积的20%硫酸溶液其质量大于10%硫酸溶液,则将溶质的质量分数为a%、物质的量浓度为C1 mol·L-1的稀硫酸加热蒸发掉溶液总质量的一半的水,此时溶质的质量分数变为b%,物质的量浓度为C2 mol·L-1,下列关系正确的是
| A.b﹤2 a | B.C2﹤2 C1 | C.C2﹥2 C1 | D.C1="2" C2 |
下列溶液中Cl-的物质的量浓度和Cl-的物质的量与50 mL 1 mol·L-1的AlCl3溶液中Cl-物质的量浓度和Cl-的物质的量都相等的是
| A.75 mL 2 mol·L-1 的NH4Cl | B.150 mL 1 mol·L-1 的NaCl |
| C.50 mL 1.5 mol·L-1 的CaCl2 | D.50 mL 3 mol·L-1 的KClO3 |
O4是意大利的一位科学家合成的一种新型的氧分子,一个分子由四个氧原子构成。振荡会发生爆炸,在大气中含量极少,在相同条件下,等质量的O4和O3比较正确的是
| A.所含原子数相等 | B.分子数之比4:3 |
| C.体积之比1:1 | D.密度之比 1:1 |