设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有C 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下22.4 L H2O所含分子数为NA |
| C.1 L 0.5 mol·L-1 CH3COOH溶液中,CH3COO-的个数为0.5NA |
| D.在NO、NO2的混合气体22.4 L中,含有的氮原子数为NA个 |
下列所述事实与化学(或离子)方程式不相符的是( )
A.能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+ 2Fe3++2H2O 2Fe3++2H2O |
B.能说明NH3结合H+能力比H2O强:NH3+H3O+ N N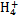 +H2O +H2O |
C.能说明盐酸是强酸:2HCl+CaCO3 CaCl2+CO2↑+H2O CaCl2+CO2↑+H2O |
D.能说明CH3COOH是弱电解质:CH3COO-+H2O CH3COOH+OH- CH3COOH+OH- |
在标准状况下①6.72 L CH4
②3.01×1023个HCl分子 ③13.6 g H2S
④0.2 mol NH3
下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
| A.abc | B.bcd | C.acd | D.abcd |
设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有C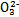 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下22.4 L H2O所含分子数为NA |
| C.1 L 0.5 mol·L-1 CH3COOH溶液中,CH3COO-的个数为0.5NA |
| D.在NO、NO2的混合气体22.4 L中,含有的氮原子数为NA个 |
下图是NaCl、MgSO4的溶解度曲线。下列说法正确的是( )。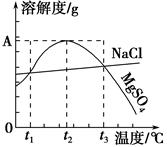
| A.只有在t1℃时,NaCl和MgSO4的溶解度才相等 |
| B.t1℃~t2℃,MgSO4的溶解度随温度升高而减小 |
| C.在t2℃时,MgSO4饱和溶液的溶质质量分数最大 |
| D.把MgSO4饱和溶液的温度从t3℃降至t2℃时,溶液的物质的量浓度减小 |
在T ℃时,将a gNH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含有NH的物质的量为b mol。下列叙述中正确的是( )。
A.溶质的质量分数为w=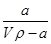 ×100% ×100% |
B.溶质的物质的量浓度c=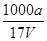 mol·L-1 mol·L-1 |
C.溶液中c(OH-)=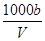 mol·L-1 mol·L-1 |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5 w |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )。
| A.将NA个HCl分子溶于500 mL水中得到2.0 mol·L-1的盐酸 |
| B.在加热条件下,100 mL 18.4 mol·L-1的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92NA |
| C.密闭容器中,1 mol SO2与0.5 mol O2充分反应,转移的电子数小于2NA |
| D.用惰性电极电解AgNO3溶液,产生11.2 L O2时,转移2 mol电子 |
下表为四种溶液的溶质质量分数和物质的量浓度的数值,根据表中数据判断四种溶液中密度最小的是( )。
| 溶液 | KOH | HNO3 | CH3COOH | HCl |
| 溶质质量分数w(%) | 56 | 63 | 60 | 36.5 |
| 物质的量浓度c(mol·L-1) | 14.3 | 13.8 | 10.6 | 11.8 |
A.HCl B.HNO3 C.CH3COOH D.KOH
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )。
| A.2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA |
| B.1 mol Na2CO3晶体中含CO32—离子数小于1NA |
| C.惰性电极电解食盐水,若线路中通过1NA电子电量,则阳极产生气体 11.2 L |
| D.0.1 mol的CaO2中含阴离子数是0.2NA |
下列叙述正确的是(双选)( )。
| A.1 mol·L-1 NaCl溶液含有NA个Na+ |
| B.10 mL质量分数为98%的H2SO4用水稀释至100 mL,H2SO4的质量分数应大于9.8% |
| C.配制240 mL 1 mol·L-1的NaOH溶液需称NaOH固体的质量为10.0 g |
| D.配制1 mol·L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 |