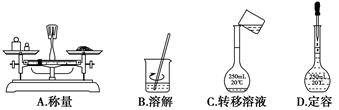
在100 mL HNO3和H2SO4的混合溶液中,加入100 mL 0.2 mol/L Ba(OH)2溶液后,pH变为7,同时生成2.33 g白色沉淀,则原混合溶液中HNO3的物质的量浓度为( )
| A.0.1 mol/L | B.0.2 mol/L |
| C.0.3 mol/L | D.0.4 mol/L |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A.25 ℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氮原子数为0.2NA |
| C.10 L pH=1的硫酸溶液中含有的H+为2NA |
| D.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
有硫酸镁溶液500 mL,它的密度是1.20 g/cm3,其中镁离子的质量分数是4.8%,则有关该溶液的说法不正确的是( )
| A.溶质的质量分数是24.0% |
| B.溶液的物质的量浓度是2.4 mol/L |
| C.溶质和溶剂的物质的量之比是1∶40 |
| D.硫酸根离子的质量分数是19.2% |
下列溶液中,溶质的物质的量浓度为1 mol/L的是( )
| A.将40 g NaOH溶于1 L水所得的溶液 |
| B.将80 g SO3溶于水并配成1 L的溶液 |
| C.将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 |
| D.含K+为2 mol的K2SO4溶液 |
下列解释事实的方程式不准确的是 ( )。
| A.用浓盐酸检验氨:NH3+HCl=NH4Cl |
B.碳酸钠溶液显碱性:CO32—+H2O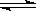 HCO3—+OH- HCO3—+OH- |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
| D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
设NA为阿伏加德罗常数的值。下列叙述正确的是 ( )。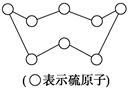
| A.3 mol NF3与水完全反应生成HNO3和NO,转移电子数2NA |
| B.标准状况下,32 g硫(结构见图)含SS的数目为NA |
| C.标准状况下11.2 L正戊烷所含共用电子对数为8NA |
| D.含a mol·L-1 H+的醋酸溶液稀释10倍后,c(H+)为0.1a mol·L-1 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温下,4 g CH4含有NA个C—H共价键 |
| B.1 mol Fe 与足量的稀HNO3反应,转移2NA个电子 |
| C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1NA个HCO3— |
| D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |
设N0为阿伏加德罗常数的值。下列叙述正确的是( )。
| A.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0 |
| B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0 |
| D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0 |