下列说法错误的是( )
| A.元素周期表共有18个纵行 |
| B.元素周期表共有7个横行,即7个周期,其中第一、二、三、四周期为短周期 |
| C.原子最外层电子数为2的元素不一定在ⅡA族 |
| D.14462Sm与14562Sm互为同位素 |
下列有关化学用语的表示正确的是( )
A.S2-的结构示意图为: |
| B.质子数为53、中子数为78的碘原子:13153I |
C.F-的结构示意图: |
| D.由含有2个中子的氢原子与10个中子的氧原子形成的水分子的化学式可表示为:21H2188O |
如图,同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2,进行喷泉实验。经充分反应后,瓶内溶质的物质的量浓度为( )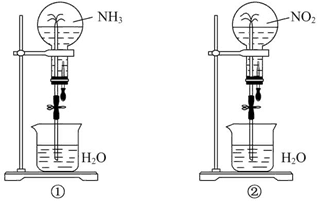
| A.①>② | B.①<② |
| C.①=② | D.不能确定 |
阿伏加德罗常数为NA,下列说法中正确的是( )
| A.62 g Na2O溶于水后所得溶液中含有的O2-数为NA |
| B.在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA |
| C.常温常压下,16 g甲基(—13CH3)所含的中子数为10NA |
| D.0.5 mol Cu和足量浓硝酸反应可以生成22.4 L NO2 |
两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42—,若将2.83 g X中的Cr3+全部氧化为Cr2O72—后,溶液中的Cr2O72—可和过量KI溶液反应,得到3.84 g I2。反应的离子方程式为Cr2O72—+6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83 g X的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀,由此可推断出X的化学式为( )
| A.K2SO4·Cr2(SO4)3 | B.2K2SO4·Cr2(SO4)3 |
| C.K2SO4·2Cr2(SO4)3 | D.K2SO4·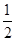 Cr2(SO4)3 Cr2(SO4)3 |
下列表述与化学用语正确的是( )
A.CO2的比例模型 |
| B.氢化铵的电子式:[H∶N?,?H,H ∶H]+H- |
| C.CH3—CH—CH—CH—CH2CH3CH3C2H5CH3的名称:2,3二甲基4乙基己烷 |
| D.二氧化硅的分子式SiO2 |
设阿伏加德罗常数的值为NA,下列说法正确的是( )
| A.标准状况下,22.4 L一氯甲烷和二氯甲烷的混合物所含氯原子数介于NA至2NA之间。 |
| B.1 mol的Cu在一定条件下与足量硫粉反应,转移电子数目为2NA |
| C.3.65 g液态氯化氢中分子的数目为0.1NA |
| D.常温下5.6 g铁投入足量的浓硝酸中,转移的电子数为0.3NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| B.在熔融状态下,1 mol NaHSO4完全电离出的阳离子数为2NA |
| C.78 g Na2O2固体与H2O完全反应转移的电子数为NA |
| D.5.6 g铁粉在2.24 L(标准状况)氯气中充分燃烧,失去的电子数为0.3NA |
设NA为阿伏加德罗常数的数值,若等质量的H2O和D2O分别与一定质量的金属钾完全反应,转移的电子数均为 NA,则下列各量不相等的是( )
NA,则下列各量不相等的是( )
| A.消耗H2O和D2O的物质的量 |
| B.同温同压下生成气体的体积 |
| C.反应后所得溶液中溶质的质量分数 |
| D.参加反应的钾的质量 |
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
| A.1 mol NaHSO4晶体含有2NA个离子 |
| B.1 L 2 mol/L明矾溶液经水解可得到氢氧化铝胶体粒子的数目为2NA |
C.1 mol C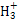 (碳正离子)中含有的电子数为10NA (碳正离子)中含有的电子数为10NA |
| D.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA |