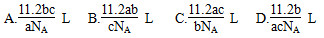NA为阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,5.6 L氯气和16.8 L氧气的混合气体中含有分子数为NA |
| B.标准状况下,22.4 LH2O所含有原子数为3NA |
| C.NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D.1 mol Na2O2与H2O完全反应,转移2NA个电子 |
a mol FeS与b mol FeO投入到V L、c mol·L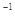 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 ( )
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 ( )
①(a+b)×63 g②(a+b)×189 g ③(a+b) mol④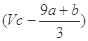 mol
mol
| A.①④ | B.②③ | C.①③ | D.②④ |
室温时,在体枳相同的容器内混合下列气体。混合后压强最小的是 ( )
| A.100mL H2和50mL O2 | B.100mL N2和200mL O2 |
| C.100mL NO和100mL O2 | D.100mL HCl和100mL NH3 |
下列叙述正确的是 ( )
A.1 mol N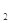 参加氧化还原反应时电子转移数为3×6.02×10 参加氧化还原反应时电子转移数为3×6.02×10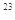 |
B.常温常压下,22.4L SO2含分子的个数为6.02×10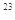 |
C.物质的量浓度为0.5 mol·L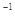 的MgCl 的MgCl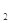 溶液,含有的Cl 溶液,含有的Cl 数为6.02×10 数为6.02×10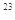 |
D.16g O2所含氧原子个数为6.02×10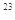 |
下列叙述中正确的是( )
| A.相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 |
| B.标准状况下,28 g CO和22.4 L SO3所含分子数相等 |
| C.5.6 g铁粉与足量氯气充分反应,有0.2 mol电子转移 |
| D.等物质的量的CH5+和NH2—所含电子数相等 |
下列指定微粒的数目相等的是( )
| A.物质的量相等的H2O与D2O含有的中子数 |
| B.20 mL NH3和30 mL O2所含的原子数 |
| C.等物质的量的Na2O和Na2O2中含有的阴离子总数 |
| D.等物质的量的钠和铜分别与氯气完全反应,转移的电子数 |
由C16O和C18O组成的混合气体与同温、同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是( )
| A.混合气体中C16O与C18O的分子数之比为14?:15 |
| B.混合气体中C16O与C18O的物质的量之比为1?:1 |
| C.混合气体中C16O与C18O的质量之比为15?:14 |
| D.混合气体中C16O与C18O的密度之比为1?:1 |
设NA表示阿伏加德罗常数的数值,下列判断正确的是( )
| A.常温常压下,22.4 L CH4中含有的C—H键数为4NA |
| B.4.6 g由NO2和N2O4组成的混合气体中含有的氧原子数为0.3NA |
| C.含0. 2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA |
| D.1 mol Na在足量O2中燃烧生成Na2O2,钠失去的电子数为NA |