设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
| B.6.8g液态KHSO4中含有0.1NA个阳离子 |
| C.标况下的NO2气体22.4L,其中含有的氮原子数为NA |
| D.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
以NA代表阿伏加德罗常数的值,下列说法申正确的是
| A.9g18O2含有的中子数为5NA |
| B.标准状况下,0.5NABr2所占的体积约为11.2L |
| C.常温下,1L0.1mol·L-1NH4NO3溶液中含有的NH4+数为0.1NA |
| D.一定条件下,lmol N2和3mol H2在密闭容器充分反应,生成N-H键的数目为6NA |
下列化学用语正确的是
| A.乙醇的结构筒式:C2H6O |
B.CH4的比例模型: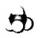 |
C.工业上制取粗硅的化学方程式:SiO2+C Si+CO2↑ Si+CO2↑ |
| D.电解饱和食盐水的离子方程式:Cl-+2H2O=Cl2↑+2OH-+H2↑ |
有0.4 g铁的氧化物,用足量的CO在高温下将其还原,把生成的CO2全部通入足量澄清石灰水中,得到0.75 g沉淀。这种铁的氧化物的化学式是( )
| A.FeO | B.Fe2O3 |
| C.Fe3O4 | D.FeO和Fe2O3 |
在硫酸、明矾和硫酸铝组成的混合溶液中,c(Al3+)="0.3" mol·L-1,c(SO42-)=0.7mol·L-1, 由水电离的c(H+)=10-13 mol·L-1,则c(K+)为
| A.0.15mol·L-1 | B.0.2mol·L-1 | C.0.3mol·L-1 | D.0.4mol·L-1 |
加热21.2g KOH和KHCO3的混合物使其充分反应后冷却,称得固体质量减少1.8g,则
下列说法中正确的是(n表示物质的量)
| A.n(KOH) = 0.1mol | B.n(KOH) < n(KHCO3) |
| C.n(KHCO3) = 0.2mol | D.n(KOH) > n(KHCO3) |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.32g甲醇中含有C-H键的数目为4NA |
| B.1L0.1mol·L-1的氨水含有0.1NA个OH- |
| C.10L pH=1的硫酸溶液中含有的H+数为2NA |
| D.H2S和SO2气体混合生成0.3mol单质硫时,转移电子的数目为0.4NA |
下列说法正确的是
| A.汽油、花生油都是油脂 |
| B.碘元素遇淀粉溶液变蓝色 |
C.质子数为86、中子数为51的铯原子: |
D.CO2的电子式: |
设nA为阿佛加德罗常数的数值,下列说法正确的是( )
| A.等物质的量的H2和N2所含分子数均为nA |
| B.标准状况下,11.2L的己烷含有分子数为0.5nA |
| C.常温常压下,46gNO2含有原子数为3nA |
| D.1mol SiO2晶体中含nA个SiO2分子 |
以NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA |
| B.28gCO中所含的原子数为2NA |
| C.1L 0.1mol/LNa2CO3溶液中,含有CO32— 数为0.1NA |
| D.22.4LH2的分子数为NA |