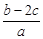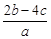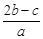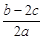设nA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |
设N0为阿伏加德罗常数的值。下列叙述正确的是( )。
| A.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0 |
| B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0 |
| D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0 |
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是 ( )。
| A.该原子的摩尔质量是aNA g |
B.W g该原子的物质的量一定是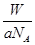 mol mol |
C.W g该原子中含有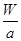 ×NA个该原子 ×NA个该原子 |
D.由已知信息可得:NA=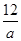 |
下列化学用语表示正确的是 ( )。
A.Cl-的结构示意图: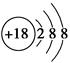 |
B.甲烷分子的球棍模型: |
C.氢氧化钠的电子式: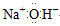 |
| D.次氯酸的结构式:H—O—Cl |
在硫酸铝、硫酸钾和明矾[KAl(SO4)2·12H2O]混合溶液中,SO42—浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为( )
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.9mol/L |
将钠、镁、铝各0.1 mol分别放入 足量盐酸中,同温同压下产生气体的体积比是
| A.3∶1∶1 | B.6∶3∶2 | C.1∶2∶3 | D.1∶1∶1 |
下列溶液中的Cl-浓度与100 mL 1 mol ·L-1 MgCl2溶液中的Cl-浓度相等的是
| A.150 mL 1 mol·L-1 AlCl3溶液 | B.75 mL 0.5mol·L-1CaCl2溶液 |
| C.150 mL 0.75 mol·L-1 CaCl2溶液 | D.75 mL 2 mol ·L-1NaCl溶液 |
用NA表示阿伏加德罗常数的值。下列说法正确的是
| A.1 L 1 mol·L-1 CuCl2溶液中含有的氯离子数为NA |
| B.常温常压下,11.2 L氢气气体中含有的分子数为0.5NA |
| C.1 mol氯气与足量的水完全反应转移的电子数为2NA |
| D.标准状况下,1 mol乙烷和乙烯的混合气中含有的碳原子数为2NA |
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是
| A.称量 | B.溶解 | C.转移 | D.定容 |