设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA |
B.标准状况下,2.24L氯气中含有的 Cl数目一定为0.2NA Cl数目一定为0.2NA |
| C.常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA |
| D.80mL 10mol·L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA |
下列有关化学用语表示正确的是
| A.乙醇的结构简式 C2H6O |
B.氨基的电子式 |
C.镁离子的结构示意图 |
D.中子数为79、质子数为55 的铯(Cs)原子 Cs Cs |
NA为阿伏伽德罗常数。下列说法正确的是( )
| A.同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B.32gCu与S完全反应转移的电子数为NA |
| C.1L 1.0mol·L-1NH4Cl与2L 0.5mol·L-1NH4Cl溶液含NH4+数目相同 |
| D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA |
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H—1 C—12)
| A.1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C.28 g聚乙烯含有的碳原子数为2NA |
| D.1 mol CH5+所含电子数为8NA |
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是
| A.Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同 |
| B.SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强 |
| C.H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO |
| D.根据常温下铜与浓硝酸可以制取NO2,推出常温下铁与浓硝酸也可以制取NO2 |
设NA表示阿伏加德罗常数。下列叙述正确的是
| A.常温常压下,22 g CO2中含有NA个C=O键 |
| B.标准状况下,将22.4L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA |
| C.常温常压下,22.4 L N2和O2的混合气体中含有的分子数目为NA |
| D.9 g重水含有的电子数为5 NA |
下列化学用语正确的是
| A.I-131:7853I |
| B.乙烯的结构简式:CH2CH2 |
C.Cl-的结构示意图: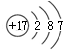 |
D.Na2S的电子式: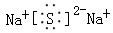 |
元素周期表里金属元素和非金属元素分界线附近能找到
| A.制农药元素 | B.制催化剂元素 |
| C.制半导体元素 | D.制耐高温合金元素 |
下列叙述能肯定金属A 比金属B更活泼的是
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子的电子层数比B原子多 |
| C.1 mol A从酸中置换出H2比1 mol B多 |
| D.常温下,A能从酸中置换出氢气,而B不能 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CO2和H2 | C.NaCl和HCl | D.CCl4和KCl |