下列化学用语的书写,正确的是
A.氮气的电子式: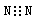 | B.硫离子的结构示意图: |
C.溴化钠的电子式: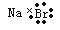 | D.水分子的球棍模型: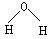 |
下列有关说法正确的是
| A.9.2 g NO2气体中含有分子数目为0.2NA |
| B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA |
| C.2 g DO中含中子、质子、电子数目均为NA |
| D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA |
下列化学用语表述正确的是( )
A.CH3COONH4的电离方程式为: CH3COONH4 CH3COO-+NH4+ CH3COO-+NH4+ |
B.NaHS的水解方程式为: HS-+H2O S2-+H3O+ S2-+H3O+ |
| C.用过量的氨水吸收SO2的离子方程式为: 2NH3·H2O+SO2=2NH4++SO32-+H2O |
| D.过量Fe粉与Cl2反应的化学方程式为: Fe +Cl2FeCl2 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.在标况下, 11.2 L NO与11.2 L O2混合后所含分子数为0.75NA |
| B.常温常压下,16 g O3所含的电子数为8NA |
| C.0.1 mol Na2O2晶体中含有0.4NA个离子 |
| D.铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A.标准状况下2.24 L己烷中,分子数为0.1NA |
| B.22.4LCl2含有Cl-Cl键数为NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A.1 mol Na2O2中含有的阴离子数为0.2NA |
| B.标准状况下,由H2O2制得2.24LO2转移的电子数目为0.4NA |
| C.常温常压下,8gO3含有4 NA个电子 |
| D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA |
下列说法正确的是( )
| A.煤的干馏和石油的分馏均属化学变化 |
| B.酯类和糖类均能发生水解反应 |
| C.生活中常见的石英玻璃、陶瓷都属于硅酸盐产品 |
| D.合金材料都是导体,可能含有非金属元素 |
NA代表阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol Cl2参加的任何反应转移电子数都是2NA |
| B.标准状况下,22.4mL水中含有的分子数目约为1.24NA |
| C.常温常压下,29g乙基(—C2H5)所含电子数为13NA |
| D.0.1 mol Na2O2中含有离子总数为0.4 NA |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA |
| B.常温下,10 L pH=12的Na2CO3溶液中含有的OH-离子数为0.1NA |
| C.标准状况下,22.4 LNO2和NO的混合气体中所含的氮原子总数为2NA |
| D.将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为 NA |
对于相应化学用语的推论合理的是( )
| 选项 | 化学用语 | 推论 |
| A | 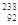 U3+ U3+ | 该铀离子核外有89个电子 |
| B | 2H2(g)+O2(g)=" " 2H2O(g);△H=-483.6kJ?mol | 1mol氢气完全燃烧放出热量483.6kJ. |
| C | 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 2NaOH+H2↑+Cl2↑ | NaCl氧化性比Cl2强 |
| D | FeO+4H++NO3―= Fe3++NO2↑+2H2O | 氧化亚铁溶于稀硝酸的离子方程式 |