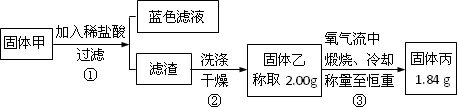
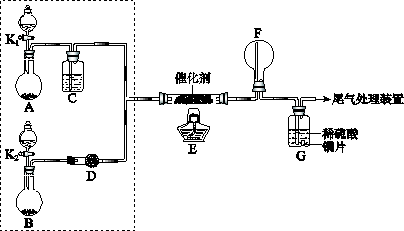
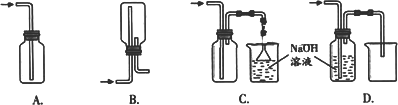
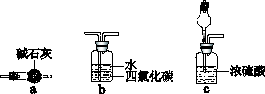0 95820 95828 95834 95838 95844 95846 95850 95856 95858 95864 95870 95874 95876 95880 95886 95888 95894 95898 95900 95904 95906 95910 95912 95914 95915 95916 95918 95919 95920 95922 95924 95928 95930 95934 95936 95940 95946 95948 95954 95958 95960 95964 95970 95976 95978 95984 95988 95990 95996 96000 96006 96014 203614