0 95689 95697 95703 95707 95713 95715 95719 95725 95727 95733 95739 95743 95745 95749 95755 95757 95763 95767 95769 95773 95775 95779 95781 95783 95784 95785 95787 95788 95789 95791 95793 95797 95799 95803 95805 95809 95815 95817 95823 95827 95829 95833 95839 95845 95847 95853 95857 95859 95865 95869 95875 95883 203614




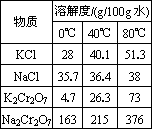
 已知:①4FeO·Cr2O3+8Na2CO3+7O2
已知:①4FeO·Cr2O3+8Na2CO3+7O2