|
浓度均为0.1 mol·L-1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是 | |
| [ ] | |
A. |
BaCl2 NaOH NaHCO3 |
B. |
Na2CO3 MgCl2 H2SO4 |
C. |
AlCl3 NH3·H2O NaOH |
D. |
Ba(OH)2 CaCl2 Na2SO4 |
|
以NA表示阿佛加德罗常数,下列说法中正确的是 | |
| [ ] | |
A. |
53 g碳酸钠中含NA个CO32- |
B. |
0.1 mol OH-含NA个电子 |
C. |
1.8 g重水(D2O)中含NA个中子 |
D. |
标准状况下11.2 L臭氧中含NA个氧原子 |
|
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是 | |
| [ ] | |
A. |
Ba2+、NO |
B. |
Ca2+、HCO |
C. |
K+、Ba2+、Cl-、HSO |
D. |
Mg2+、NH |
|
由短周期元素组成的中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是
| |
| [ ] | |
A. |
若D与盐酸反应,可生成A和B,则X一定是H2O |
B. |
若D是一种强碱,则A、B、C均可与X反应生成D |
C. |
若D为NaCl,且A可与C反应生成B,则E可能是CO2 |
D. |
若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是 | |
| [ ] | |
A. |
20 mL 10mol·L-1的浓硝酸或浓硫酸与足量铜加热反应转移电子数均为0.2NA |
B. |
0.1 mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA |
C. |
在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
D. |
标准状况下,2.24 L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
|
下列离子方程式不正确的是 | |
| [ ] | |
A. |
用稀硫酸除去铜绿:4H++Cu2(OH)2CO3 |
B. |
将Na2O2固体投入H218O中:2H218O+2Na2O2 |
C. |
向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO 2Ba2++NH |
D. |
向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO |
|
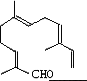
从甜橙的芳香油中可分离得到如下结构的化合物:
现在试剂:①KMnO4酸性溶液;②H2/Ni;③Ag(NH3)2OH;④新制Cu(OH)2,能与该化合物中所有官能团都发生反应的试剂有 | |
| [ ] | |
A. |
①② |
B. |
②③ |
C. |
③④ |
D. |
①④ |
|
有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀.反应中消耗x mol H2SO4、y mol AgNO3.据此得知原混合溶液中的c(Na+)/mol·L-1为 | |
| [ ] | |
A. |
(y-2x)/a |
B. |
(y-x)/a |
C. |
(2y-2x)/a |
D. |
(2y-4x)/a |
|
在pH=1时,可大量共存且形成无色溶液的一组离子或分子是 | |
| [ ] | |
A. |
Ca2+、CH3COOH、Br-、Na+ |
B. |
NO |
C. |
HClO、Ba2+、Na+、Cl- |
D. |
K+、Cl-、Al3+、SO |
|
能正确表示下列反应的离子方程式是 | |
| [ ] | |
A. |
碳酸氢钙溶液和氢氧化钠溶液混合HCO |
B. |
醋酸钠溶液和盐酸混合 CH3COONa+H+ |
C. |
少量金属钠放入冷水中Na+2H2O |
D. |
硫酸铜溶液和氢氧化钡溶液混合 Cu2++SO |