题目内容
|
在pH=1时,可大量共存且形成无色溶液的一组离子或分子是 | |
| [ ] | |
A. |
Ca2+、CH3COOH、Br-、Na+ |
B. |
NO |
C. |
HClO、Ba2+、Na+、Cl- |
D. |
K+、Cl-、Al3+、SO |

 阅读快车系列答案
阅读快车系列答案|
在pH=1时,可大量共存的无色溶液的一组离子或分子是 | |
| [ ] | |
A. |
Ca2+、CH3COOH、Br-、Na+ |
B. |
NO3-、Fe3+、Mg2+、SO42- |
C. |
ClO3-、Ba2+、Na+、Cl- |
D. |
K+、Cl-、Al3+、SO32- |
(9分)以下是25℃时几种难溶电解质的溶解度:
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子.例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可.
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe3+、Fe2+都被转化为____________(填化学式)而除去.
(2)①中加入的试剂应该选择________为宜,其原因是__________________.
(3)②中除去Fe3+所发生的总反应的离子方程式为_____________________.
(4)下列与方案③相关的叙述中,正确的是________(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
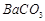 、
、 、
、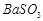 、
、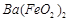 等]。某化工厂主要生产
等]。某化工厂主要生产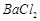 、
、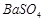 ,现利用钡泥制取
,现利用钡泥制取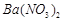 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)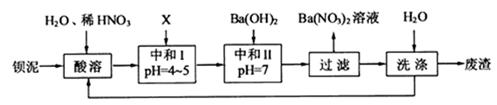
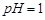 ,
,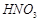 的反应化学方程式为:
的反应化学方程式为: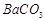 、
、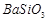 、
、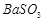 、
、 等]。某化工厂主要生产
等]。某化工厂主要生产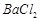 、
、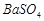 ,现利用钡泥制取
,现利用钡泥制取 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3
(2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3
(2)Fe3+在pH=3.7时即可水解即沉淀完全) 
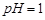 ,
,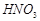 的反应化学方程式为:
的反应化学方程式为: