|
如图所示是典型氯碱工业的关键设备——离子交换膜电解槽,该电解槽的特点是用离子交换膜将槽分隔为左右两室,它能够阻止一些物质通过,也能允许一些物质通过.下列有关说法正确的是
| |
| [ ] | |
A. |
离子交换膜的特点是允许气体分子通过,而不允许阴离子通过 |
B. |
图中X是指氧气 |
C. |
电解槽右室的电极反应式为2H+→H2↑+2e- |
D. |
电解槽左室也称为阴极室 |
|
下列推论正确的是 | |
| [ ] | |
A. |
S(g)+O2(g) |
B. |
C(石墨,s) |
C. |
NaOH(aq)+HCl(aq) |
D. |
CaCO3(s) |
|
在一定条件下,当64 g SO2气体被氧化成SO3气体时,共放出热量98.3 kJ,已知SO2在此条件下转化率为80%,据此,下列热化学方程式正确的是 | |
| [ ] | |
A. |
SO2(g)+ |
B. |
2SO2(g)+O2(g) |
C. |
SO2(g)+ |
D. |
2SO2(g)+O2(g) |
|
灰锡(以粉末状存在)和白锡是锡的两种同素异形体.已知: ①Sn(s、白)+2HCl(aq) ②Sn(s、灰)+2HCl(aq) ③Sn(s、灰) | |
| [ ] | |
A. |
ΔH1>ΔH2 |
B. |
锡在常温下以灰锡状态存在 |
C. |
灰锡转化为白锡的反应是放热反应 |
D. |
锡制器皿长期处于低于13.2℃的环境中,会自行毁灭 |
|
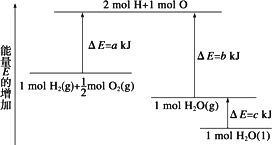
一定条件下,化学反应2H2+O2
| |
| [ ] | |
A. |
H2(g)+ |
B. |
2H2(g)+O2(g) |
C. |
H2(g)+ |
D. |
2H2(g)+O2(g) |
|
下列说法中正确的是 | |
| [ ] | |
A. |
SO2(g)+ |
B. |
2SO2(g)+O2(g) |
C. |
X(g)+Y(g) |
D. |
X(g)+Y(g) |
|
已知: (1)Fe2O3(s)+ (2)C(s)+O2(g) 则2Fe(s)+ | |
| [ ] | |
A. |
-824.4 kJ/mol |
B. |
-627.6 kJ/mol |
C. |
-744.7 kJ/mol |
D. |
-169.4 kJ/mol |
|
已知:①NH3(g)+HCl(g) ②NH3(g) ③HCl(g) ④NH3(aq)+HCl(aq) 则NH4Cl(s) | |
| [ ] | |
A. |
16.3 |
B. |
-16.3 |
C. |
335.7 |
D. |
-335.7 |
|
已知H2的燃烧热为285.8 kJ/mol,CO的燃烧热为282.8 kJ/mol.现有H2和CO组成的混合气体56.0 L(标准状况),经充分燃烧后,放出的总热量为710.0 kJ,并生成液态水.下列说法正确的是 | |
| [ ] | |
A. |
CO燃烧的热化学方程式为:2CO(g)+O2(g) |
B. |
H2燃烧的热化学方程式为:2H2(g)+O2(g) |
C. |
燃烧前混合气体中,H2的体积分数为40% |
D. |
燃烧后的混合气体与足量的过氧化钠反应,转移电子的物质的量为2 mol |
|
已知:①1 mol H2分子中化学键断裂时需要吸收436 kJ的能量;②1 mol Cl2分子中化学键断裂时需要吸收243 kJ的能量;③由H原子和Cl原子形成1 mol HCl分子时释放431 kJ的能量,下列叙述正确的是 | |
| [ ] | |
A. |
氢气和氯气反应生成氯化氢气体的热化学方程式是:H2(g)+Cl2(g) |
B. |
氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH=183 kJ/mol |
C. |
氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH=-183 kJ/mol |
D. |
氢气和氯气反应生成1 mol氯化氢气体,反应的ΔH=183 kJ/mol |