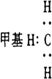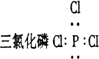|
常用的锌锰干电池在放电时总反应可表示为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,放电时负极区发生的物质或微粒是 | |
| [ ] | |
A. |
MnO2 |
B. |
MnO2和NH4+ |
C. |
Zn |
D. |
Zn2+和NH3 |
|
关于Na2CO3溶液和NaHCO3溶液,下列说法正确是是 | |
| [ ] | |
A. |
用加热的方法区别两种溶液 |
B. |
用澄清的石灰水区别两种溶液 |
C. |
浓度相同时,Na2CO3溶液的pH大 |
D. |
浓度相同时,两溶液的pH相等 |
|
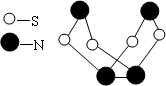
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图所示是已合成的最著名的硫-氮化合物的分子结构.下列说法正确的是
| |
| [ ] | |
A. |
该物质的分子式为SN |
B. |
该物质的分子中既有极性键,又有非极性键 |
C. |
该物质在固态时形成原子晶体 |
D. |
该物质与化合物S2N2互为同素异形体 |
|
1 mg锎( | |
| [ ] | |
A. |
锎元素的相对原子质量为252 |
B. |
|
C. |
|
D. |
|
|
甲、乙、丙为二、三周期的元素,原子序数依次增大,甲和乙同周期,甲和丙同族,甲、乙原子序数之和与丙的原子序数相等,甲、丙原子的最外层电子数之和与乙原子的电子总数相等.下列说法中,不正确的是 | |
| [ ] | |
A. |
乙是地壳中含量最多的元素 |
B. |
丙的氢化物比甲的氢化物热稳定性强 |
C. |
乙与丙形成的化合物可制作光导纤维 |
D. |
甲、乙两种元素形成的化合物中一定含有共价键 |
|
在100 mL 18.5 mol/L的浓硫酸中加入一定量的锌,充分反应后,锌完全溶解,同时生成33.6 L气体(标准状况,假设SO2全部逸出).将反应后的溶液稀释到1 L,测得溶液的pH=1,则下列叙述错误的是 | |
| [ ] | |
A. |
生成的气体是SO2和H2的混合物 |
B. |
反应的锌为97.5 g |
C. |
生成的气体中SO2和H2的体积比为1∶3 |
D. |
反应中共转移电子3 mol |
|
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠已知该电池放电时的电极反应式为:正极FePO4+Li++e- | |
| [ ] | |
A. |
充电时电池反应为FePO4+Li=LiFePO4 |
B. |
充电时动力电池上标注“+”的电极应与外接电源的正极相连 |
C. |
放电时,在正极上是Li+得电子被还原 |
D. |
放电时电池内部Li+向负极移动 |
|
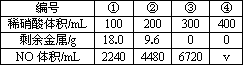
铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
下列计算结果正确的是 | |
| [ ] | |
A. |
硝酸的浓度为4 mol/L |
B. |
①中溶解了5.6 g Fe |
C. |
②中溶解了9.6 g Cu |
D. |
④中v>8960 |