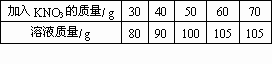|
“喷水溶液法”是最近日本科学家研制出的一种使沙漠变绿洲的技术,它是先在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙土粒子结合,在地表下30~50 cm处形成一个厚0.5 cm的隔水层,既能阻止地下的盐分上升,又有拦截、蓄积雨水的作用,下列对聚丙烯酸酯不正确的说法是 | |
| [ ] | |
A. |
单体的结构简式为CH2 |
B. |
在一定条件下能发生加成反应 |
C. |
在一定条件下能发生水解反应 |
D. |
没有固定熔沸点 |
|
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是 | |
| [ ] | |
A. |
Cu2S既是氧化产物又是还原产物 |
B. |
5 mol FeS2发生反应,有10 mol电子转移 |
C. |
产物中的SO42-离子有一部分是氧化产物 |
D. |
FeS2只作还原剂 |
|
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质.根据上述观点,下列说法不正确的是 | |
| [ ] | |
A. |
CaO2的水解产物是Ca(OH)2和H2O2 |
B. |
NaClO的水解产物之一是HClO |
C. |
PCl3的水解产物是PH3和HClO |
D. |
Mg3N2水解生成NH3和Mg(OH)2 |
|
某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是 ①有晶体析出 ②c[Ca(OH)2]增大 ③pH不变 ④c(H+)c(OH-)的积不变 ⑤c(H+)一定增大 | |
| [ ] | |
A. |
① |
B. |
①⑤ |
C. |
①②④ |
D. |
①③ |
|
钛被誉为“太空金属”,其原因是它的强度大、密度小、抗腐蚀性能好.室温下,它不与水、稀硫酸、稀硝酸反应,但易溶于氢氟酸,推断其原因 | |
| [ ] | |
A. |
氟离子易与钛离子形成可溶性难电离物质 |
B. |
氢氟酸的氧化性比其它酸强 |
C. |
氢氟酸的还原性比其它酸强 |
D. |
氢氟酸的酸性比其它酸强 |
|
一定温度下,在质量都是50 g的五份水中分别加入30 g、40 g、50 g、60 g、70 gKNO3固体,充分搅拌后,滤去未溶解的KNO3.加入的KNO3质量与相应所得溶液的质量数据见下表:则该温度下KNO3的溶解度是
| |
| [ ] | |
A. |
60克 |
B. |
80克 |
C. |
100克 |
D. |
110克 |
|
把SO2通入Fe(NO3)3溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀.在上述一系列变化过程中,最终被还原的是 | |
| [ ] | |
A. |
SO2 |
B. |
Cl- |
C. |
Fe3+ |
D. |
NO3- |
|
向含下列微粒的溶液中,①HS-、②Fe2+、③ | |
| [ ] | |
A. |
①② |
B. |
②③ |
C. |
①④ |
D. |
③④ |
|
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸.当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量B跟氯气反应除生成C外,另一产物是盐酸盐.
| |
| [ ] | |
A. |
当X是强酸时,ABCDEF均含有一种元素,F是硫酸 |
B. |
当X是强碱时,ABCDEF均含同一种元素,F是硝酸 |
C. |
B和Cl2的反应是氧化还原反应 |
D. |
当X是强酸时,C常温下是气态单质 |
|
在环境检测中常用检气管法来测定空气中S02的含量,原理是S02与KIO3发生反应,用一种有机物作指示剂,其可能反应如下(未配平): ①KIO3+SO2+H2O→I2+H2SO4+KHSO4 ②KIO3+SO2+H2O→KI+H2SO4 则下列说法正确的是 | |
| [ ] | |
A. |
检气管法是按照反应①原理设计的 |
B. |
检气管法是按照反应②原理设计的 |
C. |
反应①②均可以设计成检气管法,但考虑到相同量KIO3①消耗SO2少,所以检气管法是按①设计的 |
D. |
反应①②均可以设计成检气管法,但考虑到相同量KIO3②消耗SO2多,所以检气管法是按②设计的 |