|
有一在空气中放置了一段时间的KOH固体,经分析测知其含水2.8%、含K2CO337.3%.取1 g该样品投入25 mL 2 mol/L的盐酸中后,多余的盐酸用1.0 mol/L KOH溶液30.8 mL恰好完全中和,蒸发中和后的溶液可得到固体 | |
A. |
1 g |
B. |
3.725 g |
C. |
0.797 g |
D. |
2.836 g |
|
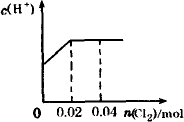
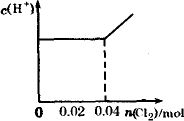
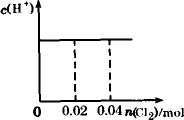
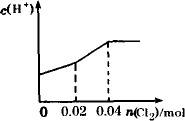
将0.03 mol Cl2缓缓通入含0.02 mol H2SO3和0.02 mol HBr的溶液中,在此过程中,溶液中的c(H+)与Cl2用量的关系示意图是(溶液的体积视为不变) | |
A. |
|
B. |
|
C. |
|
D. |
|
|
24 mL浓度为0.05 mol/L的Na2SO3溶液恰好与20 mL浓度为0.02 mol/L的K2Cr2O7溶液完全反应.已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为 | |
A. |
+2 |
B. |
+3 |
C. |
+4 |
D. |
+5 |
|
有关钠的叙述正确的是 | |
A. |
将4.6 g金属钠投入95.4 g蒸馏水中反应后,得8%的氢氧化钠溶液 |
B. |
制取过氧化钠所用的空气必须经碱石灰处理才能与钠反应 |
C. |
钠和钠离子都属于碱金属元素,所以都具有强还原性 |
D. |
钠跟酒精反应比水缓和,所以销毁残钠要用酒精处理 |
|
取17.4 g MnO2固体粉末与一定体积的浓盐酸(含溶质0.4 mol)共热制取氯气,已知反应如下:MnO2+4HCl(浓) | |
A. |
反应过程中MnO2作催化剂 |
B. |
盐酸完全反应 |
C. |
参加反应的盐酸有一半被氧化 |
D. |
反应产生2.24 L氯气(标准状况) |
|
标准状况下,往100 mL 0.2 mol/L的FeBr2溶液中通入一定体积的Cl2,充分反应后,溶液中有50%的Br-被氧化.则通入的氯气的体积是 | |
A. |
0.224 L |
B. |
0.336 L |
C. |
0.448 L |
D. |
0.672 L |
|
在反应11P+15CuSO4+24H2O | |
A. |
1/5 mol |
B. |
2/5 mol |
C. |
3/5 mol |
D. |
11/5 mol |