|
下列关于原电池的叙述中,错误的是 | |
A. |
构成原电池的正极和负极必须是两种不同的金属 |
B. |
原电池是将化学能转化为电能的装置 |
C. |
在原电池中,电子流出的一级是负极,发生氧化反应 |
D. |
原电池放电时,电流的方向是从负极到正极 |
|
关于用水制取二级能源氢气,以下研究方向不正确的是 | |
A. |
构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源 |
B. |
设法将太阳光聚焦,产生高温,使水分解产生氢气 |
C. |
寻找高效催化剂,使水分解产生氢气,同时释放能量 |
D. |
寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气 |
|
下列说法正确的是 | |
A. |
物质发生化学反应都伴随着能量变化 |
B. |
伴有能量变化的物质变化都是化学变化 |
C. |
在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 |
D. |
在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
|
一定温度下,有可逆反应:2A(g)+2B(g)C(g)+3D(g);△H<0.现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入体积为2V的乙容器.关于两容器中反应的说法正确的是 | |
A. |
甲容器中的反应先达到化学平衡状态 |
B. |
两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同 |
C. |
两容器达平衡后升高相同的温度,达到新的平衡,甲乙容器中平衡混合物中各组份的体积百分组成不同 |
D. |
在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 |
|
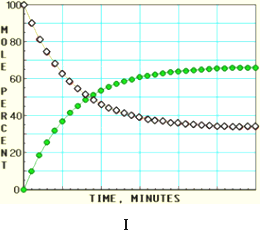
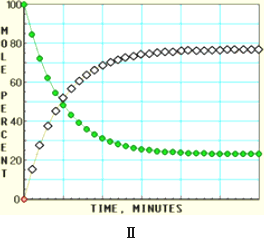
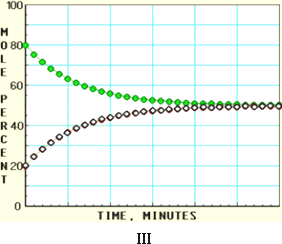
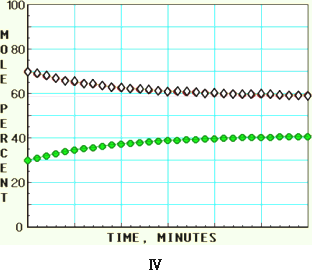
随着信息技术的迅猛发展,计算机在化学化工领域得到了广泛应用.下面四幅图是用计算机制作的在密闭容器里,在不同条件下进行反应:X(g)
下列有关说法正确的是 | |
A. |
图中的纵坐标表示物质的物质的量分数 |
B. |
四幅图中,图Ⅲ所示反应达到平衡时,X的转化率为37.5% |
C. |
图Ⅰ和图Ⅱ所采用的不同条件是反应体系压强不同 |
D. |
图Ⅳ说明反应开始时是向正反应方向进行的 |
|
在一定条件下化学反应:N2(g)+3H2(g)
根据以上数据,下列叙述一定不正确的是 | |
A. |
在上述条件下反应生成1 mol NH3气体放热46.2 kJ |
B. |
2Q2<2Q3<Q1<92.4 |
C. |
Q1=2Q2=2Q3=92.4 |
D. |
若丙改为恒压容器,其它条件不变,则有Q2<Q3 |
|
已知甲为恒温恒压容器,乙为恒温恒容容器.初始时,两容器的温度、体积相同,两容器中均充入2 mol SO2和l mol O2,且发生反应为2SO2(g)+O2(g) | |
A. |
向甲容器中再充人一定量的氦气 |
B. |
向乙容器中再充人2 mol的SO3气体 |
C. |
适当降低乙容器的温度 |
D. |
缩小甲容器的体积 |