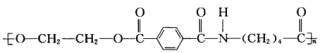
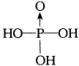
溴乙烷(CH3CH2Br)是一种难溶于水,密度约为水的密度的1.5倍,沸点为38.4℃的无色液体,实验室由乙醇制溴乙烷的反应如下:![]() ;
;![]() 已知反应物的用量:0.3mol NaBr(固体);0.25mol乙醇;36ml浓硫酸(98%,密度1.84g/cm3);25ml水,其中乙醇的密度约为水的密度的4/5。试回答:
已知反应物的用量:0.3mol NaBr(固体);0.25mol乙醇;36ml浓硫酸(98%,密度1.84g/cm3);25ml水,其中乙醇的密度约为水的密度的4/5。试回答:
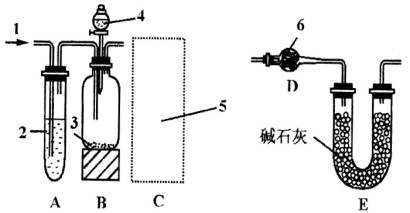
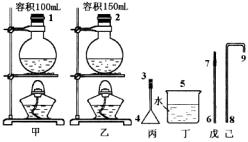
(1)仅用下图所示仪器来安装制取和收集溴乙烷的装置,要求达到安全、损失少、不污染环境的目的。有关仪器的选择和连接顺序为____________(填数字)。
(2)在表中写出不能选用的仪器及理由(填仪器代码,如:甲、乙……不一定填满)。
|
不能使用的仪器 |
理由 |
|
|
|
|
|
|
|
|
|
(3)反应时,若温度过高,可见有棕色气体生成,写出此反应的化学方程式:______。
(4)从棕黄色的粗溴乙烷制取无色的溴乙烷应加入的试剂是__________,必须使用的仪器是___________。
(5)本实验的产率为60%,则可制取溴乙烷____________g。
现有Fe、Cu组成的合金,其中Fe、Cu的总物质的量为a mol,Cu的物质的量分数为x。将合金研成粉末后,全部投入到含b mol HNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)用粒子符号填写下列空白(列举出全部可能的情况)
|
|
① |
② |
③ |
④ |
… |
|
残留固体成分 |
|
|
|
|
|
|
溶液中的金属离子 |
|
|
|
|
|
⑵当溶液中金属离子只有Fe2+和Cu2+时,则b的取值范围是 ___ (用a、x表示)。
⑶当x=0.5时,溶液中Fe2+与Fe3+的物质的量相等时,在标准状况下共产生672 mL气体。求a、b的值。