|
设NA表示阿伏加德罗常数,下列叙述中正确的是 | |
| [ ] | |
A. |
3.4 g NH3中含N-H键数目为0.2NA |
B. |
27 g Al在22.4 L Cl2中燃烧,转移的电子总数为3NA |
C. |
0.5 mol·L-1 CuCl2溶液中含Cl-数为NA |
D. |
84 g NaHCO3与MgCO3的混合物中所含氧原子数目为3NA |
|
A、B、C均为短周期元素,A、B同周期, A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构,下列说法中正确的是 | |
| [ ] | |
A. |
C元素的最高正价为+7价 |
B. |
原子半径:A>B>C |
C. |
离子半径:A2->C->B2+ |
D. |
还原性:A2-<C- |
|
下图中a、b、c、d、e为元素周期表中前4周期的一部分元素,下列有关叙述正确的是
| |
| [ ] | |
A. |
b元素除0价外,只有一种化合价 |
B. |
五种元素中,c元素的性质最稳定 |
C. |
相同条件下b和d气态氢化物溶于水,溶液的酸性:d<b |
D. |
e元素最高价氧化物的水化物和不同量的氧氧化钠溶液反应,可能生成三种盐 |
|
下列各组离子在指定溶液中一定能大量共存的是: | |
| [ ] | |
A. |
加入铝有氢气放出的溶液中:Ca2+、K +、HCO3-、Cl- |
B. |
碱性的溶液中:Fe2+、ClO-、Na+、SO42- |
C. |
使紫色石蕊试液变红的溶液中:NH4+、AlO2-、K +、SO42- |
D. |
酸性溶液中:Fe3+、MnO4-、NO3-、Na+ |
|
下列说法中正确的是: ①所有基态原子的核外电子排布都遵循构造原理 ②同一周期从左到右,元素的第一电离能、电负性都是越来越大 ③分子中键能越大,表示分子拥有的能量越高 ④所有的配合物都存在配位键,所有含配位键的化合物都是配合物 ⑤所有含极性键的分子都是极性分子 ⑥熔融状态下能导电的化合物一定是离子化合物 ⑦所有的原子晶体都不导电 | |
| [ ] | |
A. |
①② |
B. |
①⑥ |
C. |
③④⑤ |
D. |
⑥ |
|
2008的秋天,毒奶粉事件震惊全国,这主要是奶粉中含有有毒的三聚氰胺,下列关于三聚氰胺分子的说法中正确的是
| |
| [ ] | |
A. |
一个分子中共含有15个σ键 |
B. |
所有碳原子采用sp2杂化,所有氮原子采用sp3杂化 |
C. |
属于极性分子,故极易溶于水 |
D. |
形成的晶体熔点较高 |
|
已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是 | |
| [ ] | |
A. |
A、B、D不可能在同周期 |
B. |
C和D的单质可能化合为离子化合物 |
C. |
D一定在第二周期 |
D. |
A、D可能在同一主族 |
|
下列说法中正确的是 | |
| [ ] | |
A. |
C60气化和金刚石熔化克服的作用力相同 |
B. |
甲酸甲酯的熔点低于乙酸的熔点 |
C. |
氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 |
D. |
分子晶体的熔沸点低,常温下均呈液态或气态 |
|
已知锂和镁的单质及其化合物在很多性质上具有相似性,由此可以推断下列关于锂及其化合物的叙述中,正确的是 | |
| [ ] | |
A. |
LiOH加热时,不会分解 |
B. |
Li2CO3加热时,不会分解 |
C. |
Li在氧气中燃烧生成Li2O2 |
D. |
Li与稀硫酸反应生成Li2SO4 |
|
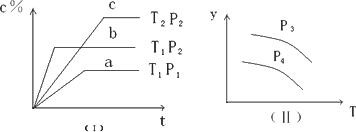
在某密闭容器中,可逆反应:A(g)+B(g)
| |
| [ ] | |
A. |
P3>P4,y轴表示A的百分含量 |
B. |
P3<P4,y轴表示B的百分含量 |
C. |
P3<P4,y轴表示混合气体的密度 |
D. |
P3>P4,y轴表示混合气体的平均相对分子质量 |