|
由Na2O2、Na2CO3、NaHCO3、NaCl中某几种组成的混合物,向其中加入足量的盐酸有气体放出.将气体通过足量的NaOH溶液,气体体积减少一部分.将上述混合物在空气中加热,有气体放出,下列判断正确的是 | |
| [ ] | |
A. |
混合物中一定不含有Na2CO3、NaCl |
B. |
混合物中一定有Na2O2、NaHCO3 |
C. |
无法确定混合物中是否含有NaHCO3 |
D. |
混合物中一定不含Na2O2、NaCl |
|
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-226 kJ/mol 根据以上热化学方程式判断,下列说法正确的是 | |
| [ ] | |
A. |
CO的燃烧热为283 kJ |
B. |
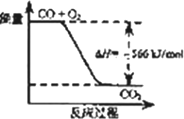
下图可表示由CO生成CO2的反应过程和能量关系
|
C. |
2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol |
D. |
CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
|
下列排列顺序正确的是 ①固体的热稳定性:CaCO3>Na2CO3>NaHCO3 ②还原性:SO32->I->Br- ③微粒半径:K+>Na+>O2- ④结合H+的能力:OH->AlO2->HCO3- ⑤氢化物的沸点:H2O>NH3>HF | |
| [ ] | |
A. |
①③ |
B. |
②④ |
C. |
①② |
D. |
③⑤ |
|
三聚氰酸C3N3(OH)3可用于消除汽车尾气中的氮氧化物.当加热至一定温度时,它分解产生的HNCO(异氰酸,其结构是H-N=C=O)能和NO2反应:HNCO+NO2 | |
| [ ] | |
A. |
N2是还原产物,CO2是氧化产物质 |
B. |
每生成1 mol CO2需转移12 mol电子 |
C. |
反应中氧化剂和还原剂的物质的量之比为3∶2 |
D. |
N元素既被氧化也被还原 |
|
关于ⅠA族和ⅡA族元素的下列说法中正确的是 | |
| [ ] | |
A. |
加热时,Na2CO3比MgCO3易分解 |
B. |
浓度都是0.01 mol·L-1时,KOH溶液的pH比Ba(OH)2的小 |
C. |
Na的熔点比Mg高,Na2O的熔点比MgO的高 |
D. |
NaOH是一元碱,Mg(OH)2是二元碱,后者碱性强 |
|
下列叙述中正确的是 | |
| [ ] | |
A. |
在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物 |
B. |
由于碱金属形成的碱均为强碱,所以碱金属形成的盐均不会水解 |
C. |
金属锂不能保存于煤油中,金属钾可以保存于煤油中 |
D. |
做焰色反应时应用硫酸洗铂丝 |
|
在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后,恢复到原来的温度,下列说法中正确的是 | |
| [ ] | |
A. |
溶液的pH不变,有H2放出 |
B. |
溶液的pH值增大,有O2放出 |
C. |
溶液中c(Na+)增大,有O2放出 |
D. |
溶液中Na+数目减少,有O2放出 |
|
关于Na2CO3溶液和NaHCO3溶液,下列说法正确的是 | |
| [ ] | |
A. |
用加热的方法区别两种溶液 |
B. |
用澄清的石灰水区别两种溶液 |
C. |
浓度相同时,Na2CO3溶液的pH大 |
D. |
浓度相同时,两溶液的pH相等 |