(16分)(相对原子质量:Na 23 O 16 H 1)
(1)配制物质的量浓度为0.2 mol/L的NaOH溶液500 mL,填空并请回答下列问题:
|
应称量NaOH的质量/g |
已给仪器 |
除已给仪器外还需要的其他仪器 |
|
|
烧杯、药匙、 托盘天平 |
|
(2)下列操作对配制的NaOH溶液浓度有偏高影响的是_______
A.称量NaOH固体时,露置在空气的时间过长
B.选用的容量瓶内有少量的蒸馏水
C.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
D.在定容时仰视容量瓶刻度线
(3)向0.1 mol/L的AlCl3溶液中加入过量的0.2 mol/L的NaOH溶液,则发生反应的离子方程式为
(4)将配制好的0.2 mol/L的NaOH溶液逐滴加入到0.1 mol/L的Ca(HCO3)2溶液中,则发生反应的离子方程式为
(16分)已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃。
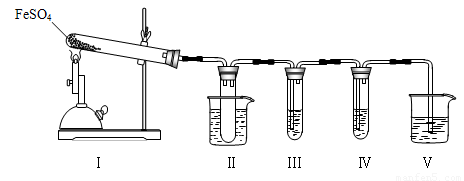
(1)装置Ⅱ的试管中不装任何试剂,其作用是______________________
试管浸泡在50℃的水浴中,目的是______________________________
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。
限选试剂:3 mol·L-1 H2SO4、6 mol·L-1 NaOH、0.5 mol·L-1 BaCl2、0.5 mol·L-1 Ba(NO3)2、
0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水。
|
检验试剂 |
预期现象和结论 |
|
装置Ⅲ的试管中加入__________ ___。 |
产生大量白色沉淀,证明气体产物中含有SO3。 |
|
装置Ⅳ的试管中加入_______ _________。 |
______________________________ ______________________________ ______________________________ ______________________________ |
(3)装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是 。




 FeO(s)+CO(g)
△H1= a kJ·mol-1
FeO(s)+CO(g)
△H1= a kJ·mol-1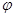 为混合物中CO含量,T为温度)。
为混合物中CO含量,T为温度)。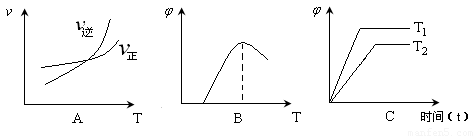
 的说法正确的是
的说法正确的是