题目内容
(16分)在密闭容器中进行:
反应① Fe(s)+CO2(g)  FeO(s)+CO(g)
△H1= a kJ·mol-1
FeO(s)+CO(g)
△H1= a kJ·mol-1
反应② 2CO(g)+O2(g)  2CO2(g)
△H2= b kJ·mol-1
2CO2(g)
△H2= b kJ·mol-1
反应③ 2Fe(s)+O2(g)  2FeO(s)
△H3
2FeO(s)
△H3
(1)△H3= (用含a、b的代数式表示)
(2)反应①的化学平衡常数表达式K= ,已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为 ,CO的平衡浓度为
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.再通入CO2
C.升高温度 D.使用合适的催化剂
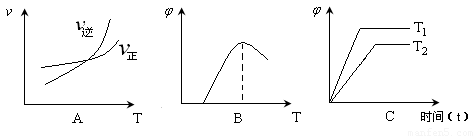
(4)下列图像符合反应①的是 (填序号)(图中ν是速率、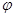 为混合物中CO含量,T为温度)。
为混合物中CO含量,T为温度)。
【答案】
(16分)
(1)(2a+b)kJ·mol-1(2分)(没有单位扣1分)
(2)c(CO)/c(CO2)(2分);50% (2分);0.5 mol·L-1 (2分)
(3)>(2分);BC(4分,漏选1个扣2分,错选/多选均不得分)
(4)C(2分)
【解析】

练习册系列答案
相关题目
在密闭容器中进行X2(g)+4Y2(g)?2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别是0.1mol?L-1、0.4mol?L-1、0.2mol?L-1、0.3mol?L-1当反应达到平衡后,各物质的物质的量浓度不可能是( )
| A、c(X2)=0.15 mol?L-1 | B、c(Y2)=0.9 mol?L-1 | C、c(Z2)=0.3 mol?L-1 | D、c(Q2)=0.5 mol?L-1 |
 2NO在密闭容器中进行,下列哪些条件能加快反应的速率( )
2NO在密闭容器中进行,下列哪些条件能加快反应的速率( ) 已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )