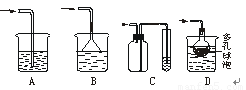
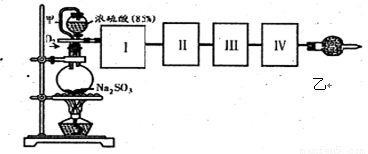
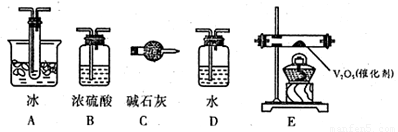
根据下列实验现象,所得结论正确的是( )

|
实验 |
实验现象 |
结论 |
|
A. |
左烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Mg>Cu |
|
B. |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C. |
左边溶液产生黄色沉淀,右边溶液产生黄色沉淀 |
氧化性:Cl2>Br2>S |
|
D. |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:S>C>Si |
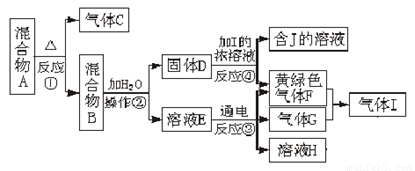
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
 ①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;④ H2MoO4====MoO3+H2O;
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一釉强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
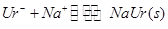 ,第一次关节炎发作往往在冬季,有关该反应的说法正确的是
,第一次关节炎发作往往在冬季,有关该反应的说法正确的是