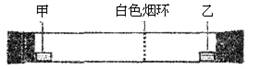
(9分)某同学对MnO2、CuO、Fe2O3、Cr2O3在氯酸钾受热分解反应中的催化作用进行了研究。实验所得数据如下表。就本实验的有关问题,请填空:
|
实验 编号 |
KClO3(g) |
氧化物 |
产生气体(mL) (已折算为标况) |
耗时(s) |
||
|
化学式 |
质量(g) |
实际回收 |
||||
|
1 |
0.6 |
— |
— |
— |
10 |
480 |
|
2 |
0.6 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.6 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.6 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.6 |
Cr2O3 |
0.20 |
异常 |
67.2 |
188.3 |
(1)本实验的装置由下图三部分组成,其正确的接口连接顺序为 。
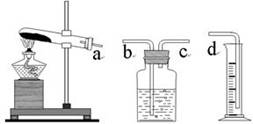
(2)为证明编号2的实验中MnO2起到催化作用,上述实验后还要测定反应剩余物MnO2的质量,实验的操作顺序是:溶解→ → → → 。
(3)从上表实验数据分析,对氯酸钾受热分解有催化作用的物质,按其催化能力从大到小的顺序为 (填物质的化学式)。
(4)从编号3的实验数据,可计算出KClO3的分解率为 %(保留一位小数)。
(5)在进行编号5的实验时,有刺激性的黄绿色气体产生,该气体可能是______(填化学式),常用 试纸检验该气体,上述异常现象产生的原因是 。


 2HI(g) △H=-9.48 kJ/mol
2HI(g) △H=-9.48 kJ/mol 
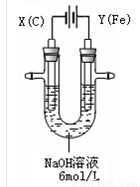
 Pb+PbO2+2H2SO4,则它在充电时的阳极反应为
Pb+PbO2+2H2SO4,则它在充电时的阳极反应为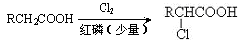
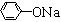 +RCl
+RCl
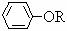 +NaCl
+NaCl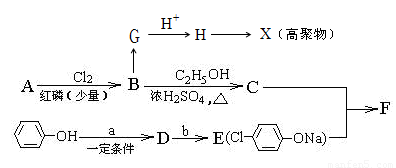
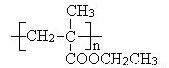 ),反应的化学方程式是:
),反应的化学方程式是: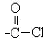 结构)。
结构)。