题目内容
(15分)已知:
Ⅰ. 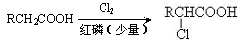
Ⅱ. 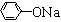 +RCl
+RCl
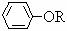 +NaCl
+NaCl
冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
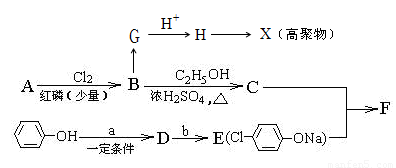
(1)A是饱和一元羧酸,8.8gA与足量NaHCO3溶液反应生成 2.24L(标准状况)CO2,则A的分子式为 。
(2)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B水解生成化合物G的反应方程式: 。
(3)写出H ® X的化学方程式: 。
(4)D的苯环上有两种氢,其结构简式是 ,D具有的性质有 。
A. 可以发生消去反应、取代反应
B. 可以发生加成反应、氧化反应
C. 在一定条件下,与氢氧化钠反应,最多消耗2molNaOH
D. 能与FeCl3溶液发生显色反应
(5)写出C ® F的化学方程式: 。
(6)聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维。若用上述物质中的C通过2步反应合成高聚物Y(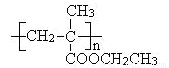 ),反应的化学方程式是:
),反应的化学方程式是:
第一步: ;
第二步: 。
(7)与B互为同分异构体的属于酯类的化合物共有
种(不含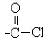 结构)。
结构)。
(1)C4H8O2
 (2)
(2)
(3)n

 +(n-1)H2O
+(n-1)H2O
(4)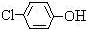 BCD
BCD
(5)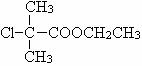 +
+

 +NaCl
+NaCl
(6)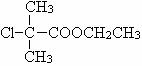 +NaOH
+NaOH
 +NaCl+H2O
+NaCl+H2O

(7)11
【解析】(1)CO2是0.1mol,则饱和一元羧酸的物质的量是0.1mol,因此羧酸的相对分子质量是88。-COOH的相对分子质量是45,所以取代基的相对分子质量是43,即为丙基,所以分子式为C4H8O2。
(2)B是氯代羧酸,其核磁共振氢谱有两个峰,所以B的结构简式为(CH3)2CClCOOH,其水解反应方程式为 。B的同分异构体中,属于酯类,说明必须含有-COO-。若是甲酸形成的酯,则相应的醇可以是丙醇,丙醇有正丙醇和异丙醇,其中氯原子的位置友5种情况。若是乙酸形成的酯,则氯原子的位置有三种,。若是丙酸形成的酯,则氯原子也有3种情况,所以共有11种同分异构体。
。B的同分异构体中,属于酯类,说明必须含有-COO-。若是甲酸形成的酯,则相应的醇可以是丙醇,丙醇有正丙醇和异丙醇,其中氯原子的位置友5种情况。若是乙酸形成的酯,则氯原子的位置有三种,。若是丙酸形成的酯,则氯原子也有3种情况,所以共有11种同分异构体。
(3)G酸化即得到H,因此H中既含有羧基,也含有羟基,可以发生缩聚反应生成高分子化合物,方程式为 。
。
(4)根据E的结构简式可知,D中含有氯原子。苯环上有两种氢,所以结构简式是 。苯环上的氯原子不能发生消去反应,所以A是错误的。答案选BCD。
。苯环上的氯原子不能发生消去反应,所以A是错误的。答案选BCD。
(5)B和乙醇发生酯化反应生成C,则C的结构简式为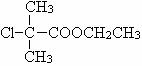 。所以C和F反应的方程式为
。所以C和F反应的方程式为
 。
。
(6)要合成高聚物Y,则必须有单体 ,C通过消去反应即得到该单体,所以加聚即得到Y,反应式为
,C通过消去反应即得到该单体,所以加聚即得到Y,反应式为
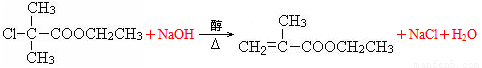 、
、
 。
。

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:
通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验: (2011?双流县模拟)已知反应:3A(g)+B(g)
(2011?双流县模拟)已知反应:3A(g)+B(g) C(s)+4D(g);△H=-Q kJ/lmol下列分析错误的是( )
C(s)+4D(g);△H=-Q kJ/lmol下列分析错误的是( )