在温度相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知CO(g)+2H2(g) CH3OH(g) ΔH=-90.7 kJ/mol):
CH3OH(g) ΔH=-90.7 kJ/mol):
|
容器 |
甲 |
乙 |
丙 |
|
反应物投入量 |
1 mol CO、2 mol H2 |
1 mol CH3OH |
2 mol CH3OH |
|
CH3OH的浓度(mol/L) |
c1 |
c2 |
c3 |
|
反应的能量变化 |
放出a kJ |
吸收b kJ |
吸收c kJ |
|
平衡时压强(Pa) |
P1 |
P2 |
P3 |
|
反应物转化率 |
α1 |
α2 |
α3 |
下列说法不正确的是
A.c1=c3 B.a+c/2<90.7 C.2P2>P3 D.α1+α3=1
(12分)原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36。已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
|
电离能/kJ·mol—1 |
I1 |
I2 |
I3[来源:] |
I4[来源:ZXXK] |
|
X |
496 |
4562 |
6912 |
9543 |
|
Y |
738 |
1451 |
7733 |
10540 |
|
Z |
578 |
1817 |
2745 |
11578 |
(1)X、Y、Z的电负性从大到小的顺序为 (用元素符号表示),元素Y的第一电离能大于Z的原因是 。
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输。已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示。
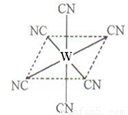
①W元素基态原子价电子排布式为 。
②已知CN—与 分子互为等电子体,1molCN—中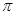 键数目为
。
键数目为
。
③上述沉淀溶解过程的化学方程式为 。
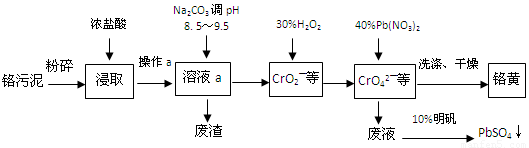
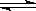 Al(OH)3 +3H+的平衡常数为
。
Al(OH)3 +3H+的平衡常数为
。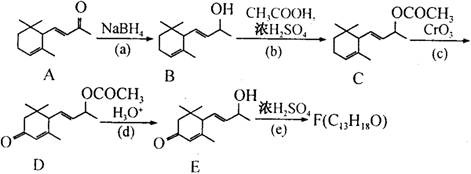
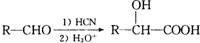 ,写出以乙醇和
,写出以乙醇和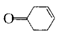 为原料制备
为原料制备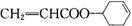 的合成路线图(无机试剂任选)。合成路线流程图示例如下:
的合成路线图(无机试剂任选)。合成路线流程图示例如下: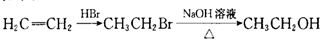
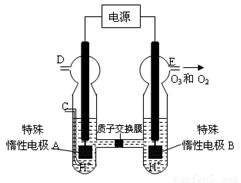
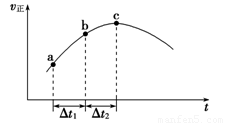
 (4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是