1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念。下表给出的是第三周期的七种元素和第四周期的钾元素的电负性的值。下列说法不正确的是( )
|
元素 |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
K |
|
电负性 |
0.9 |
1.2 |
1.5 |
? |
2.1 |
2.3 |
3.0 |
0.8 |
A 钙元素的电负性的取值范围在0.8与1.2之间
B. 硫化钠的电子式为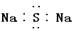
C 硅元素的电负性的取值范围 在1.5与2.1之间
D Al与S形成的化学键可能为共价键
几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
X |
Y |
Z |
W |
|
原子半径/pm |
160 |
143 |
70 |
66 |
|
主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述不正确的是
A.X、Y元素的金属性X<Y
B.X单质在空气中燃烧可以形成化合物X3Z2
C. X和Y均能与氧化物发生置换反应
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据,下列说法正确的是( )
|
元素 |
I1/eV |
I2/eV |
I3/eV |
|
甲 |
5.7 |
47.4 |
71.8 |
|
乙 |
7.7 |
15.1 |
80.3 |
|
丙 |
13.0 |
23.9 |
40.0 |
|
丁 |
15.7 |
27.6 |
40.7 |
A 甲的金属性比乙强 B 乙的化合价为+1价
C 丙一定为非金属元素 D 丁一定是金属元素

