根据下表中部分短周期元素的原子半径及主要化合价判断,下列叙述正确的是
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.075 |
0.102 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+5、+3 |
+6、-2 |
-2 |
A. 离子半径: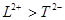
B. 氢化物的还原性:
C. M与T形成的化合物只能与盐酸反应,不与 溶液反应
溶液反应
D. 一定条件下,T的单质可将Q从其氢化物中置换出来
(6分)为了研究外界条件对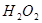 分解反应速率的影响,某同学在四支试管中分别加入
分解反应速率的影响,某同学在四支试管中分别加入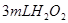 溶液,并测量收集
溶液,并测量收集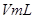 气体所需的时间,实验记录如下:
气体所需的时间,实验记录如下:
|
实验序号 |
|
|
催化剂 |
所用时间 |
|
① |
5% |
20℃ |
2滴 |
|
|
② |
5% |
40℃ |
2滴 |
|
|
③ |
10% |
20℃ |
2滴 |
|
|
④ |
5% |
20℃ |
不使用 |
|
请回答:
(1)过氧化氢分解的化学方程式是__________。
(2)实验①②是研究__________对反应速率的影响。
(3)实验测得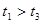 ,原因是__________。
,原因是__________。
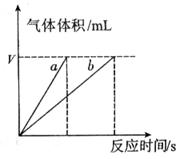
(4)实验①④的测定过程如下图,曲线a对应的实验序号是__________(填“①”或“④”)。
(12分)①~⑧是元素周期表中的部分元素。
|
周期 |
IA |
|
0 |
|||||
|
1 |
① |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
|
2 |
|
|
|
② |
|
③ |
④ |
|
|
3 |
⑤ |
⑥ |
⑦ |
|
|
|
⑧ |
|
请回答:
(1)元素③④⑧的气态氢化物中最稳定的是__________(填化学式)。
(2)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式是__________。
(3)元素⑥和⑧形成的化合物的电子式是__________。
(4)某同学为了比较元素②和硅元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。请回答:

a. X是__________(填化学式),B装置的作用是__________。
b. 能说明元素②和硅元素非金属性强弱的实验现象是__________,相关的化学方程式是__________。同主族元素从上到下__________,得电子能力逐渐减弱,非金属性逐渐减弱。
(5)请设计实验比较元素⑥与⑦金属性的相对强弱__________。

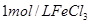
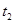
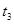
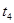
 族
族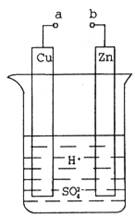
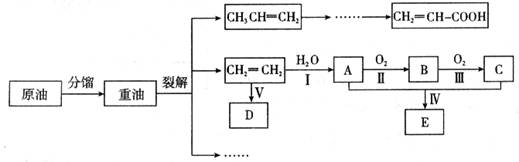
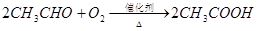

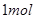 C、
C、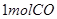 分别按下式反应(燃烧):
分别按下式反应(燃烧):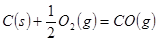 放热
放热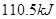
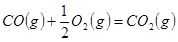 放热
放热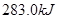
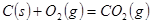 放热
放热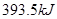
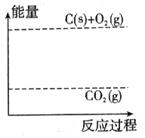

 )
)