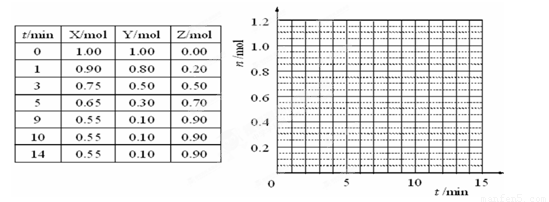
(14分)下面是18×7的格子,按要求作答。
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
He |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
D |
|
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
F |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)用封闭的实线绘出元素周期表的轮廓。注意:不得使用铅笔作图。(3分)
(2)“大爆炸理论”指出:200亿年以前,宇宙中所有物质都包含在一个密度无限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就产生了元素。你由此可知最先产生的元素是_______(填写元素名称)(1分),其中子数比质子数多1的核素的原子符号是_________;(1分)
(3)C、D、E、F的简单离子半径由小到大顺序是_______________________(填写离子符号);(2分)
(4)请用电子式表示出E和H形成的化合物形成过程:_____________________________;(2分)
(5)用实线绘出金属与非金属的分界线。注意:不得使用铅笔作图。(2分)
(6)用来组成酸、碱、盐三类物质至少需要的元素有__________(填写表中字母)。(3分)
 2PbSO4+2H2O 下列结论正确的是( )
2PbSO4+2H2O 下列结论正确的是( )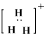
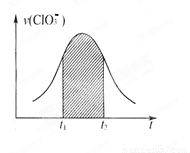
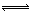 b
Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
b
Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )